
| A. | 镁用于制造轻合金,是制造飞机、火箭的重要材料 | |
| B. | 高纯度硅制成的光电池,可用作火星探测器的动力 | |
| C. | 聚脂纤维属于新型无机非金属材料,可制作宇航服 | |
| D. | 高温结构陶瓷耐高温、耐氧化,是喷气发动机的理想材料 |
分析 A.镁合金硬度大,密度小;
B.硅属于半导体材料;
C.聚酯纤维为有机高分子材料
D.高温结构陶瓷耐高温,不怕氧化、密度小.
解答 解:A.镁合金硬度大,密度小,可用于制造汽车、飞机、火箭,故A正确;
B.硅属于半导体材料,高纯度硅制成的光电池,可用作火星探测器的动力,故B正确;
C.制作航天服的聚酯纤维属于有机物,不是无机材料,属于合成有机高分子材料,故C错误;
D.高温结构陶瓷耐高温,不怕氧化、密度小,所以高温结构陶瓷时喷气发动机的理想材料,故D正确.
故选C.
点评 本题考查较为综合,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养、提高学生学习的积极性,注意相关基础知识的积累,难度不大.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | “血液透析”利用了胶体的性质 | |
| B. | 溶液是电中性的,胶体是带电的 | |
| C. | 一束光线分别通过溶液和胶体时,前者会出现明显的光带,后者则没有 | |
| D. | 浓NaOH溶液中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | |
| C | D |
| A. | 阴离子半径从大到小的排列顺序为:C>D>B | |
| B. | B元素的两种同素异形体常温下都是气体 | |
| C. | 最高价氧化物对应的水化物的酸性:D>C | |
| D. | B元素的氢化物的沸点低于C元素的氢化物的沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
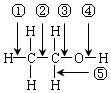 ,乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;分子间脱水生成乙醚时,断开的键是③④;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.
,乙醇与钠反应时,断开的键是④;与HX反应时,断开的键是③;分子内脱水生成乙烯时,断开的键是①③;分子间脱水生成乙醚时,断开的键是③④;在铜催化作用下发生催化氧化反应时,断开的键是④⑤;酯化反应时,断开的键是④.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
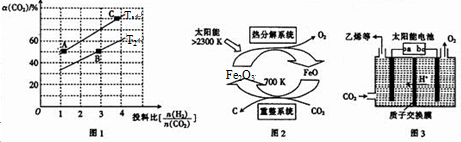
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com