
【题目】镁、铝、铁是三种重要金属,它们的单质和化合物应用十分广泛。回答下列问题:
(1)镁、铝第一电离能大小的关系是I1(Mg)___I1(Al),金属镁、铝熔点大小关系是Mg___Al。(填“大于”、“等于”或“小于”)
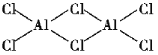
(2)氯化铝加热时易升华,实验测得铝元素与氯元素形成化合物的实际组成为Al2Cl6,其结构简式如图所示。其中处于中间的Cl原子杂化轨道类型为___杂化,分子中所有原子___(能、不能)在同一平面上。
(3)硝酸铁和尿素在乙醇中生成[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁]。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为___。尿素分子中σ键与π键的数目之比为___。NO3-的空间构型为___,经测定N2O5晶体中存在NO2+和NO3-,NO2+中氮原子为___杂化。
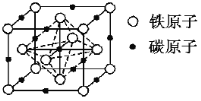
(4)碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构如图所示。晶体中与相邻铁原子距离相等且最近的铁原子有___个,该物质的化学式为___。若晶体密度为dg·cm-3,则晶胞中最近的两个碳原子的距离为___pm(阿伏加德罗常数的值为NA表示,写出简化后的计算式即可)。
【答案】大于 小于 sp3 不能 1s22s22p63s23p63d5 7:1 平面三角形 sp 12 FeC 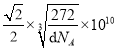
【解析】
(1)同一周期元素,其第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素;金属熔沸点与金属键强弱有关;
(2)根据结构简式判断其成键特点,分析杂化方式;
(3)Fe为26号元素,原子形成阳离子时,先失去高能层中电子,同一能层先失去高能级中电子;尿素的结构式为![]() ;根据价层电子对数判断杂化类型,根据价层电子对互斥判断空间构型;
;根据价层电子对数判断杂化类型,根据价层电子对互斥判断空间构型;
(4)以顶点Fe原子研究,与之距离最近的Fe原子处于面心,利用“均摊法”确定化学式;根据晶胞可以判断出两个碳原子的最近距离为面对角线的一半。
(1)镁失去能量较低的3s上成对电子,铝失去能量较高的3p上成单电子,故I1(Mg)大于I1 (A1);铝比镁价电子多,离子半径小,金属键强、品体熔点高,
故答案为:大于;小于;
(2)中问的Cl原子有两个σ键、孤电子对数为2,价层电子对数为4,故为sp3杂化,Al原子有4个σ键、孤电子对为0,价层电子对数为4,故为sp3杂化,与A1结合的4个Cl原子处于四面体顶点,分子中所有原子不能在同一平面上,
故答案为:sp3;不能;
(3)Fe为26号元素,原子形成阳离子时,先失去高能层中电子,同一能层先失去高能级中电子,所以基态Fe3+的核外电子排布式为1s22s22p63s23p63d5;根据尿素的结构简式可知,分子中σ键的数目为7,π键的数目1;NO3-的中心原子价层电子对数为3,没有孤电子对,故空间构型为平面三角形;NO2+的中心原子价层电子对数为2,故为sp杂化,
故答案为:1s22s22p63s23p63d5;7:1;平面三角形;sp;
(4)以顶点Fe原子研究,与之距离最近的Fe原子处于面心,每个顶点为8个晶胞共用,每个面为2个晶胞共用,故与铁原子距离最近的铁原子数目为3×8/2=12;该晶胞中8顶点和6面心有Fe原子,晶胞含有Fe原子的数目为8×1/8+6×1/2=4,12棱心和体心有碳原子,晶胞含有碳原子数目为12×1/4+1=4,Fe原子和碳原子数目最简整数比为1:1,所以化学式为FeC;晶胞边长为a pm,根据密度计算公式可知![]() ,解得
,解得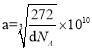 ,最近两个碳原子的距离为面对角线的一半即
,最近两个碳原子的距离为面对角线的一半即![]() ,即
,即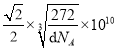
故答案为:12;FeC;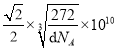 ;
;


科目:高中化学 来源: 题型:
【题目】氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液处理废水中的氰化钠。硫代硫酸钠的工业制备原理为2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并检测氰化钠废水处理后的排放情况。
I、实验室通过如图所用的装置制备Na2S2O3

(1)仪器A的名称___,使用前注意的事项___。
(2)b装置的作用是___。
(3)装置a中发生反应的化学方程式____。
(4)反应开始后,c中先有淡黄色浑浊产生,此浑浊物为___(填化学式);反应后剩余的SO2全部被d中的氢氧化钠溶液吸收,若恰好生成酸式盐,反应后的溶液呈___(“酸”或“碱”)性,原因是___。
II、已知:废水中氰化钠的最高排放标准为0.50mg/L。
(1)向氰化钠溶液中通入少量CO2能发生反应:NaCN+CO2+H2O=HCN+NaHCO3,浓度相同①NaCN、②Na2CO3、③NaHCO3三种溶液pH值由大到小的顺序(用序号表示):___。
(2)工业上常用碱性氯化法处理含氰废水,其原理如下:第一步,NaCN与NaClO反应,生成NaOCN和NaCl;第二步,NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。某工厂含氰废水中NaCN的含量为1.47mg/L,处理10m3这样的废水,理论上需要5mol/LNaClO溶液___L处理后才可以进行排放。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列四种金属堆积模型的说法正确的是( )

A.图1和图4为非密置层堆积,图2和图3为密置层堆积
B.图1~图4分别是简单立方堆积、体心立方堆积、面心立方堆积、体心立方堆积
C.图1~图4每个晶胞所含有原子数分别为1、2、2、4
D.图1~图4堆积方式的空间利用率分别为52%、68%、74%、74%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO3)是工业盐的主要成分,在漂白、电镀等方面应用广泛。己知: 室温下,2NO+Na2O2= =2NaNO2,以木炭、浓硝酸、Na2O2为主要原料制备亚硝酸钠的装置如图所示。(部分夹持装置已略去)下列说法正确的是
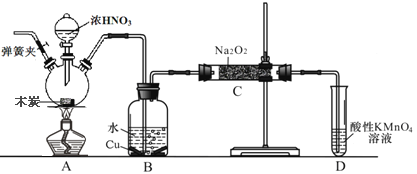
A. 实验开始前先向装置中通入N2,实验结束时先停止通入N2再熄灭酒精灯
B. 可以将B中药品换成NaOH 溶液
C. 应在B、C之间加一个盛放碱石灰的干燥管
D. D装置用于尾气处理,标况下,每吸收11.2L的尾气消耗0.2mol 的高锰酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取的乙烯中常混有少量的![]() ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
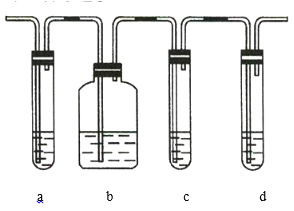
(1)图中a、b、c、d装置盛放的试剂依次是___________________(填序号)。
A.品红溶液 B.![]() 溶液 C.浓硫酸 D.酸性高锰酸钾溶液
溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明![]() 存在的实验现象是______________________________________。
存在的实验现象是______________________________________。
(3)使用装置b的目的是________________________。
(4)使用装置c的目的是________________________。
(5)能说明混合气体中含有乙烯的现象是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取的乙烯中常混有少量的![]() ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:

(1)图中a、b、c、d装置盛放的试剂依次是___________________(填序号)。
A.品红溶液 B.![]() 溶液 C.浓硫酸 D.酸性高锰酸钾溶液
溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明![]() 存在的实验现象是______________________________________。
存在的实验现象是______________________________________。
(3)使用装置b的目的是________________________。
(4)使用装置c的目的是________________________。
(5)能说明混合气体中含有乙烯的现象是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷。若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
A.CH3CH2CH2CH2CH2OH B.(CH3)2COHCH2CH3
C.(CH3)2CHCH2CH2OH D.(CH3)3CCH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气既是一种优质的能源,又是一种重要化工原料,高纯氢的制备是目前的研究热点。
(1)甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是:
CH2(g)+2H2O(g)![]() CO2(g)+4H2(g) △H=+165.0kJ·mol-1
CO2(g)+4H2(g) △H=+165.0kJ·mol-1
已知反应器中存在如下反应过程:
I.CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.4kJ·mol-1
CO(g)+3H2(g) △H1=+206.4kJ·mol-1
II.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2

根据上述信息计算:a=___、△H2=___。
(2)某温度下,4molH2O和lmolCH4在体积为2L的刚性容器内同时发生I、II反应,达平衡时,体系中n(CO)=bmol、n(CO2)=dmol,则该温度下反应I的平衡常数K值为___(用字母表示)。
(3)欲增大CH4转化为H2的平衡转化率,可采取的措施有___(填标号)。
A.适当增大反应物投料比武n(H2O):n(CH4)
B.提高压强
C.分离出CO2
(4)H2用于工业合成氨:N2+3H2![]() 2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是___。
2NH3。将n(N2):n(H2)=1:3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是___。

某温度下,n(N2):n(H2)=1:3的混合气体在刚性容器内发生反应,起始气体总压为2×l07Pa,平衡时总压为开始的90%,则H2的转化率为___,气体分压(p分)=气体总压(p总)×体积分数,用某物质的平衡分压代替物质的量浓度也可以表示化学平衡常数(记作Kp),此温度下,该反应的化学平衡常数Kp=___(分压列计算式、不化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
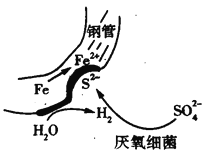
【题目】在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,有关厌氧腐蚀的机理有多种,其中一种理论为厌氧细菌可促使SO42-与H2反应生成S2-,加速钢管的腐蚀,其反应原理如图所示。下列说法正确的是( )
A. 正极的电极反应式为:2H2O+O2+4e-=4OH-
B. SO42-与H2的反应可表示为:4H2+SO42--8e S2-+4H2O
S2-+4H2O
C. 钢管腐蚀的直接产物中含有FeS、Fe(OH)2
D. 在钢管表面镀锌或铜可减缓钢管的腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com