
【题目】铅蓄电池是典型的可充电电池,电池总反应式为:[Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O.
2PbSO4+2H2O.

请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时,正极的电极反应式是_______________________________。
电解液中H2SO4的浓度将变__________,当外电路通过1 mol电子时,理论上负极板的质量增加_________,电池中消耗的硫酸物质的量为__________。
(2)在完全放电耗尽PbO2和Pb时,若按上图连接,电解一段时间后,则在A电极上生成______。B电极上生成_______,充电完成后,重新放电,A电极为________极。
【答案】PbO2+4H++SO42-+2e-=PbSO4+2H2O 小 48g 1 mol Pb PbO2 负
【解析】
(1)根据总反应式可知放电时,正极二氧化铅得到电子,电极反应式是PbO2+4H++SO42-+2e-=PbSO4+2H2O,放电时不断消耗硫酸,则溶液中硫酸的浓度将变小;负极电极反应:Pb+SO42--2e-=PbSO4,因此当外电路通过1mol电子时,理论上负极板的质量增加0.5mol×96g/mol=48g;根据总反应式可得消耗的硫酸与转移电子的关系式为:H2SO4—e-,则电池中消耗硫酸物质的量为1mol;故答案为:PbO2+4H++SO42-+2e-=PbSO4+2H2O、小、48g、1 mol;
(2)在完全放电耗尽PbO2和Pb时,电极上是析出的PbSO4,若按题图连接时,B为阳极失去电子发生氧化反应,A为阴极得到电子发生还原反应,B电极上发生反应为:PbSO4+2H2O-2e-=PbO2+4H++2SO42-,A电极发生反应为:PbSO4+2e-=Pb+SO42-,所以A电极上生成Pb;B极生成PbO2,此时铅蓄电池的正负极的极性将对换,A电极变为负极,故答案为:Pb、PbO2、负。


科目:高中化学 来源: 题型:
【题目】下列与阿伏加德罗常数的值( NA)有关的说法正确的是
A. 在标准状况下,2.24L水中含有氢原子的数目为2NA
B. 8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA
C. 在密闭容器中加入0.5 mol N2和1.5 mol H2,充分反应后可得到NH3分子数为NA
D. 2.3 g Na与氧气完全反应,反应中转移的电子数在0.1NA~0.2NA之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸钡是一种强介电化合物材料,具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”,工业制取方法如下,先获得不溶性草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧后可获得钛酸钡粉体。

(1)酸浸时发生的反应的离子方程式为__________________;
(2)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是_________________________;
(3)加入H2C2O4溶液时,发生反应的化学方程式为____________________;可循环使用的物质X是________(填化学式),设计实验方案验证草酸氧钛钡晶体是否洗涤干净:_______________________;
(4)煅烧草酸氧钛钡晶体得到BaTiO3的同时,生成高温下的气体产物有CO、_______和_________;
(5)工业上用饱和Na2CO3溶液处理重晶石(主要成分是BaSO4),待达到平衡后,移走上层清液,重复多次操作,将其转化为易溶于酸的BaCO3,再由BaCO3制备其它钡盐。已知常温下:Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.58×10-9,请问至少需要______ mol·L-1的碳酸钠溶液浸泡才能实现上述转化(忽略CO32-的水解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个电化学过程的示意图,请回答下列问题:

(1)图中甲池是_________ (填“原电池” “电解池”或“电镀池”)。
(2)A(石墨)电极的名称是_________ (填“正极” “负极” “阴极”或“阳极”)
(3)写出通入CH3OH的电极的电极反应式________________
(4)乙池中反应的化学方程式为__________________。当乙池中B(Ag)极质量增加54g,甲池中理论上消耗O2的体积为____L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn-MnO2干电池广泛应用,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是_____。电池工作时,电流流向___________(填“正极”或“负极”)
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀。请解释原因_________。欲除去Cu2+,最好选用下列试剂中的(填代号)。
A.NaOH B. Zn C. Fe D. NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阳极反应式为________。若电路中通过2 mole-,MnO2的理论产量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关甲苯的实验事实中,能说明苯环对侧链性质产生影响的是
A.甲苯燃烧产生带浓烟的火焰B.甲苯能使酸性KMnO4溶液褪色
C.甲苯的硝化反应生成三硝基甲苯D.甲苯能与H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+3/2O2(g)=SO2(g)+H2O(g)△H1
②2H2S(g)+SO2(g)=3/2S2(g)+2H2O(g)△H2
③H2S(g)+1/2O2(g)=S(g)+H2O(g)△H3
④2S(g)=S2(g)△H4
则△H4的正确表达式为( )
A. △H4=![]() (△H1+△H2-3△H3)B. △H4=
(△H1+△H2-3△H3)B. △H4=![]() (3△H3-△H1-△H2)
(3△H3-△H1-△H2)
C. △H4=![]() (△H1+△H2-3△H3)D. △H4=
(△H1+△H2-3△H3)D. △H4=![]() (△H1-△H2-3△H3)
(△H1-△H2-3△H3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]硼及其化合物用途非常广泛,回答下列问题。
(1)下列B原子电子排布图表示的状态中,能量最低和最高的分别为________、________(填标号)
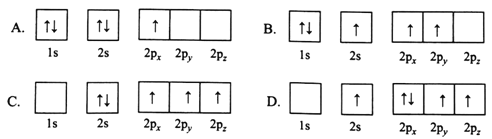
(2)H3BO3是一元弱酸,可用作医用消毒剂其水溶液呈酸性的原理为:
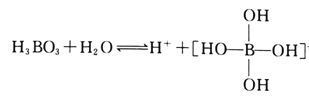
则1mol硼酸分子中含有的共用电子对数为________个。
(3)BF3可用于制造火箭的高能燃料,其分子的空间构型是________________,硼原子杂化方式是________________;BF3能与乙醚发生反应:(C2H5)2O+BF3→BF3·O(C2H5)2,该反应能发生,其原因是________________________________。
(4)硼的一种化合物结构简式为O=B—CH=C=CH2,该分子中含________个σ键。
(5)下图中图(a)为类似石墨的六方BN,图(b)为立方BN。
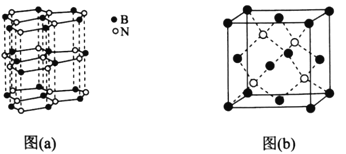
①六方BN具有良好的润滑性,是因为________________________;六方BN不能像石墨一样具有导电性,其原因是________________________。
②已知立方BN的晶胞参数为0.3615nm,阿伏加德罗常数的值为NA,则立方BN的密度为________________g·cm-3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应 2NO2(g)![]() N2O4 (g)在体积不变的密闭容器中反应,达到平衡状态的标志是
N2O4 (g)在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成 n mol N2O4 的同时生成 2n mol NO2
②单位时间内消耗 n mol N2O4的同时生成 2n mol NO2
③用NO2、N2O4的物质的量浓度变化表示的反应速率的比为2:1 的状态
④混合气体的颜色不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
A. ①④⑤B. ②⑤C. ①③④D. ①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com