
 阅读下文,回答问题.
阅读下文,回答问题. .
.分析 (1)阅读题干回答问题,常温下烷烃含4个碳为气体;
(2)甲烷高温分解得到炭黑和氢气,结合原子守恒书写化学方程式;
(3)结合甲烷结构为正四面体分析,三氯甲烷为四面体结构;
(4)丙烷化学符号为C3H8,是无色气体,纯品无臭.燃烧的火焰颜色为亮黄色,在强光和日光情况下均可识别和拍摄,燃烧产物为二氧化碳和水(蒸气);
(5)乙烷与氯气生成一氯乙烷发生取代反应;
(6)a.煤矿坑道中有易燃气体;
b.丁烷在加压条件下为液体,减压变化为常温下的气体;
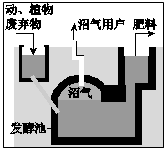
c.发酵池中主要产生沼气;
d.人们在一定的温度、湿度、pH条件下,将秸秆、杂草、人畜粪便等堆积在发酵池中,经隔绝空气发酵产生沼气.
解答 解:(1)天然气中除甲烷外,另有少量的乙烷、丙烷和丁烷,还有硫化氢、二氧化碳、氮气、水汽和少量一氧化碳等,天然气中除含甲烷外,还含有乙烷、丙烷、丁烷等有机物,
故答案为:乙烷、丙烷、丁烷;
(2)甲烷高温分解得到炭黑的化学方程式是:CH4$\stackrel{高温}{→}$ C+2H2,
故答案为:CH4$\stackrel{高温}{→}$ C+2H2;
(3)氯仿的结构式是: ,故答案为:
,故答案为: ;
;
(4)北京奥运火炬选择丙烷作气体燃料的原因是:丙烷价格低廉,可燃温度范围宽,燃烧火焰呈亮黄色易识别,燃烧产物无污染.它是一种清洁燃料等,故选abcd,
故答案为:abcd;
(5)乙烷与氯气生成一氯乙烷发生取代反应生成氯化氢和一氯乙烷,反应的化学方程式为:CH3CH3+Cl2 $\stackrel{光照}{→}$ CH3CH2Cl+HCl,
故答案为:CH3CH3+Cl2 $\stackrel{光照}{→}$ CH3CH2Cl+HCl;
(6)a.煤矿坑道中有易燃气体,遇到明火发生爆炸,需要严禁明火,故a正确;
b.丁烷在加压条件下为液体,减压变化为常温下的气体,可用作冷冻剂和气体打火机燃料,故b正确;
c.发酵池中主要成分产生沼气,还伴随有其他气体生成,故C错误;
d.人们在一定的温度、湿度、pH条件下,将秸秆、杂草、人畜粪便等堆积在发酵池中,经隔绝空气发酵产生沼气,发酵池中可利用的原料有秸秆、杂草、人畜粪便等,故d正确;
故答案为:abd.
点评 本题考查了沼气的生成和成分、烷烃性质分析判断、主要是题干信息的利用,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{w(A+x-n)}{A}$mol | B. | $\frac{A(A-x+n)}{w}$mol | C. | $\frac{w(A-x-n)}{A}$mol | D. | $\frac{w(A+x+n)}{A}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=2,b=1 | B. | a=3,b=2 | C. | a=2,b=2 | D. | a=3,b=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 阳离子 | Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀 | 9.1 | 7.6 | 1.9 |
| 完全沉淀 | 11.1 | 9.7 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 有机物A | 有机物B | 有机物C | 有机物D |
| ①可用于果实催熟 ②比例模型为  | ①由C、H两种元素组成 ②球棍模型为  | ①生活中常见的液态有机物,分子中碳原子数与有机物A相同 ②能与Na反应,但不能与NaOH反应 | ①相对分子质量比有机物C大14 ②能由有机物C氧化生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  图表示0.1molMgCl2•6H2O在空气中充分加热时固体质量随时间的变化 | |
| B. |  图表示用0.1000 mol•LˉlNaOH溶液滴定25.00 mLCH3COOH的滴定曲线,则c(CH3COOH)=0.0800 mol•Lˉ1 | |
| C. |  图表示恒温恒容条件下,2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| D. |  图表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则常温下,NaA溶液的pH小于同浓度的NaB溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①是将煤在空气中加强热使其分解的过程 | |
| B. | 煤中含有苯、甲苯、二甲笨等有机物 | |
| C. | ②是放热的过程 | |
| D. | B为甲醇或乙酸时,原子利用率均达到100% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com