
”¾ĢāÄæ”æ·Ē½šŹōĖäČ»ÖÖĄąĖäČ»²»¶ą£¬µ«ŹĒÓėČĖĄąµÄ¹ŲĻµĆÜĒŠ£¬»ŲŅä¼øÖÖ³£¼ū·Ē½šŹōŅ»¹č”¢ĀČ”¢Įņ”¢µŖ¼°Ęä»ÆŗĻĪļµÄÖŲŅŖŠŌÖŹ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ŌŚĪŽ»ś·Ē½šŹō²ÄĮĻÖŠ£¬¹čŅ»Ö±°ēŃŻ×ÅÖ÷ŅŖµÄ½ĒÉ«£¬ÓŠĻĀĮŠĪļĘ·»ņÉč±ø:¢ŁĢՓɲĶ¾ß¢Ś×©ĶߢŪĖ®ÄąĀ·ĒÅ¢ÜĆÅ“°²£Į§¢ŻĖ®¾§¾µĘ¬¢ŽČĖ¹¤ÖĘŌģµÄ·Ö×ÓÉø¢ßĀźč§ŹÖļķ¢ą¹čĢ«ŃōÄܵē³Ų¢įŹÆÓ¢¹āµ¼ĻĖĪ¬¢ā¼ĘĖ滜Š¾Ę¬”£ĖłÓĆ²ÄĮĻĪŖSiO2»ņŅŖÓƵ½SiO2µÄŹĒ_______”£
A.¢Ü¢Ż¢ß¢ą¢į B.¢Ü¢Ż¢ß¢į C.¢Ü¢Ż¢ß¢į D.¢Ł¢Ü¢Ż¢ß¢į¢ā
(2)1774Äź£¬Čšµä»Æѧ¼ŅÉįĄÕŌŚŃŠ¾æČķĆĢæóµÄ¹ż³ĢÖŠ·¢ĻÖĮĖĀČĘų”£ĻÖĪŖĮĖ½ųŠŠÓŠ¹ŲĀČĘųµÄŠŌÖŹŹµŃ飬ŠčŅŖ4ĘæČŻ»żĪŖ50mLµÄĀČĘų(ŹŅĪĀĻĀ£¬ĀČĘųµÄĆܶČŌ¼ĪŖ2.9g/L),ŌņÓĆÉįĄÕµÄ·½·ØÖĘČ”3ĘæĀČĘųĄķĀŪÉĻŠčŅŖMnO2¹ĢĢåµÄÖŹĮæŹĒ_____g(±£Įōµ½Š”ŹżµćŗóŅ»Ī»£¬ÅØŃĪĖį¹żĮ棬æÉŅŌ²¹³ä)£»Źµ¼Ź³ĘĮæµÄMnO2¹ĢĢåµÄÖŹĮæ±ŲŠė¶ąÓŚĄķĀŪĮ棬ĘäŌŅņŹĒ_____£¬ÓÉÓŚĀČĘųÓŠ¶¾£¬²š³ż×°ÖĆŹ±ŠčŅŖ¶Ō·“ӦװÖĆÄŚĀČĘų½ųŠŠ“¦Ąķ£¬ŅŌĻĀ×īĄķĻėµÄĪüŹÕ¼ĮŹĒ_____
A.NaOHČÜŅŗ B.ÅØ°±Ė® C.³ĪĒåŹÆ»ŅĖ® D.Ė®
(3)ĮņĖįŗĶĻõĖį¶¼ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ŌŚ¹¤ŅµÉĻæÉŅŌÓĆÓŚÖĘ»Æ·Ź”¢Å©Ņ©”¢ÕØŅ©”¢ŃĪĄąµČ”£
¢ŁĻÖŅŌĻ“¾»µÄ·ĻĶŠ¼ŗĶÅØĻõĖįĪŖŌĮĻ£¬ÖĘČ”ĻõĖįĶ£¬ĒėÉč¼ĘŅ»øö¼ČÄܽŚŌ¼ŌĮĻÓÖÄÜ·ĄÖ¹ĪŪČ¾»·¾³µÄ·½·Ø(ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾)____________”£
¢ŚĻĀĮŠĻÖĻóÖŠĮņĖįĖł±ķĻÖ³öµÄŠŌÖŹÖŠŗ¬ÓŠĒæŃõ»ÆŠŌµÄŹĒ________”£
A.°ŃŠæĮ£·ÅČėĻ”ĮņĖįÖŠŹ±£¬ÓŠĘųĢå·Å³ö
B.Ź¢ÓŠÅØĮņĖįµÄÉÕ±³ØæŚ·ÅÖĆŅ»¶ĪŹ±¼äŗó£¬ÖŹĮæŌö¼Ó
C.°ŃÅØĮņĖįµ¹ČėČóŹŖµÄÕįĢĒÖŠ£¬ÕįĢĒ±äŗŚ£¬ĒŅÓŠ“Ģ¼¤ŠŌĘųĪ¶ĘųĢåÉś³É
D.°ŃľĢæ·ÅČėČȵÄÅØĮņĖįÖŠŹ±£¬ÓŠĘųĢå·Å³ö
E.ŌŚ³£ĪĀĻĀæÉŅŌÓĆĢś”¢ĀĮÖĘČŻĘ÷Ź¢×°ĄäµÄÅØĮņĖį
”¾“š°ø”æ C 0.5 Éś³ÉµÄĀČĘų²»ÄÜĶźČ«ŹÕ¼Æµ½¼ÆĘųĘæÖŠ B 2Cu+O2![]() 2CuO (2·Ö) CuO+2HNO3=Cu(NO3)2+H2O CDE
2CuO (2·Ö) CuO+2HNO3=Cu(NO3)2+H2O CDE
”¾½āĪö”æ(1)¢ŁĢՓɲĶ¾ß¢Ś×©ĶߢŪĖ®ÄąĀ·ĒÅ¢ÜĆÅ“°²£Į§ŹĒ¹čĖįŃĪ²ÄĮĻ”£ ¢ÜĆÅ“°²£Į§¢ŻĖ®¾§¾µĘ¬¢ßĀźč§ŹÖļķ¢įŹÆÓ¢¹āµ¼ĻĖĪ¬ŹĒ¶žŃõ»Æ¹č²ÄĮĻ”£¢ŽČĖ¹¤ÖĘŌģµÄ·Ö×ÓÉøŹĒĀĮ¹čĖįŃĪ²ÄĮĻ”£¢ā¼ĘĖ滜Š¾Ę¬ŹĒøß“æ¹č²ÄĮĻ”£¹ŹCÕżČ·”££Ø2£©ÉčŠčŅŖµÄMnO2¹ĢĢåµÄÖŹĮæŹĒĪŖx,
MnO2+4HCl=MnCl2+Cl2+2H2
87 71
x 3”Į0.05”Į2.9
½āµĆx=0.5g ŌŚ·“Ó¦¹ż³ĢÖŠÉś³ÉµÄĀČĘųŅŖ³äĀśÕūøö×°ÖĆ£¬ĀČĘų²»ÄÜĶźČ«ŹÕ¼Æµ½¼ÆĘųĘæÖŠ£¬ĖłŅŌŠčŅŖ¼ÓČė¹żĮæµÄMnO2¹ĢĢ唣ÓÉÓŚĀČĘųÓŠ¶¾,ĪŖĮĖŌöĒæĪüŹÕŠ§¹ū£¬æÉÓĆĒæ¼īĪüŹÕ£¬¹ŹŃ”A£Ø3£©¢ŁČōŅŌĶŗĶÅØĻõĖįÖ±½Ó·“Ó¦ÖĘĻõĖįĶ£¬»į²śÉśµŖµÄŃõ»ÆĪļ£¬ĪŪČ¾æÕĘų£¬ĖłŅŌæÉŅŌĻČ°ŃĶŌŚæÕĘųÖŠŃõ»Æ³ÉŃõ»ÆĶ£¬ŌŁŗĶĻõĖį·“Ó¦£¬ÕāŃłæÉŅŌ±ÜĆāÉś³ÉµŖµÄŃõ»ÆĪļ¶ųĪŪČ¾æÕĘų£¬²¢ĒŅĢįøßĮĖĻõĖįµÄĄūÓĆĀŹ£¬·½³ĢŹ½ĪŖ£ŗ2Cu+O2![]() 2CuO CuO+2HNO3=Cu(NO3)2+H2O (6). A”¢ŠæŗĶĻ”ĮņĖį·“Ó¦£¬ŹĒĒāĄė×Ó°ŃŠæŃõ»Æ£¬Ć»ÓŠ±ķĻÖĮņĖįµÄĒæŃõ»ÆŠŌ£¬A“ķĪó”£B”¢±ķĻÖĮĖÅØĮņĖįµÄĪüĖ®ŠŌ£¬¹ŹB“ķĪó”£C”¢ÅØĮņĖįŹ¹ÕįĢĒĢ¼»Æ£¬±ķĻÖĮĖÅØĮņĖįµÄĶŃĖ®ŠŌ£¬ÕāŹĒĒæŃõ»ÆŠŌµÄŅ»ÖÖ±ķĻÖ£¬¹ŹCÕżČ·”£D”¢ÅØĮņĖį½«Ģ¼Ńõ»ÆĪŖ¶žŃõ»ÆĢ¼Ņ²ŹĒÅØĮņĖįĒæŃõ»ÆŠŌµÄŅ»ÖÖ±ķĻÖ£¬¹ŹDÕżČ·”£E”¢ŌŚ³£ĪĀĻĀæÉŅŌÓĆĢś”¢ĀĮÖĘČŻĘ÷Ź¢×°ĄäµÄÅØĮņĖįŹĒŅņĪŖĢś”¢ĀĮŌŚÅØĮņĖįÖŠ¶Ū»Æ£¬ÕāŅ²±ķĻÖĮĖÅØĮņĖįµÄĒæŃõ»ÆŠŌ£¬¹ŹEÕżČ·”£±¾ĢāÕżČ·Ń”ĻīĪŖCDE
2CuO CuO+2HNO3=Cu(NO3)2+H2O (6). A”¢ŠæŗĶĻ”ĮņĖį·“Ó¦£¬ŹĒĒāĄė×Ó°ŃŠæŃõ»Æ£¬Ć»ÓŠ±ķĻÖĮņĖįµÄĒæŃõ»ÆŠŌ£¬A“ķĪó”£B”¢±ķĻÖĮĖÅØĮņĖįµÄĪüĖ®ŠŌ£¬¹ŹB“ķĪó”£C”¢ÅØĮņĖįŹ¹ÕįĢĒĢ¼»Æ£¬±ķĻÖĮĖÅØĮņĖįµÄĶŃĖ®ŠŌ£¬ÕāŹĒĒæŃõ»ÆŠŌµÄŅ»ÖÖ±ķĻÖ£¬¹ŹCÕżČ·”£D”¢ÅØĮņĖį½«Ģ¼Ńõ»ÆĪŖ¶žŃõ»ÆĢ¼Ņ²ŹĒÅØĮņĖįĒæŃõ»ÆŠŌµÄŅ»ÖÖ±ķĻÖ£¬¹ŹDÕżČ·”£E”¢ŌŚ³£ĪĀĻĀæÉŅŌÓĆĢś”¢ĀĮÖĘČŻĘ÷Ź¢×°ĄäµÄÅØĮņĖįŹĒŅņĪŖĢś”¢ĀĮŌŚÅØĮņĖįÖŠ¶Ū»Æ£¬ÕāŅ²±ķĻÖĮĖÅØĮņĖįµÄĒæŃõ»ÆŠŌ£¬¹ŹEÕżČ·”£±¾ĢāÕżČ·Ń”ĻīĪŖCDE



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠ½šŹōµ„ÖŹA”¢B”¢CŗĶĘųĢå¼×”¢ŅŅ”¢±ūŅŌ¼°ĪļÖŹD”¢E”¢F”¢G”¢H£¬ĖüĆĒÖ®¼äµÄĻą»„×Ŗ»Æ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£ØĶ¼ÖŠÓŠŠ©·“Ó¦µÄÉś³ÉĪļŗĶ·“Ó¦µÄĢõ¼žĆ»ÓŠ±ź³ö£©”£
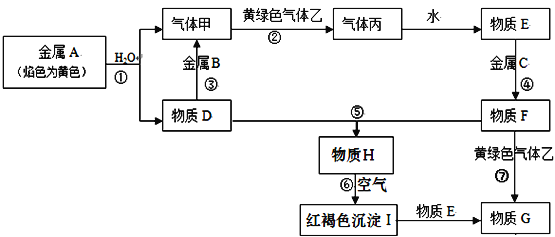
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½£ŗB_________£¬ŅŅ_________
£Ø2£©øł¾ŻŅŖĒó»Ų“š£ŗ
1)DČÜŅŗŗĶFČÜŅŗŌŚæÕĘųÖŠ»ģŗĻµÄĻÖĻó£ŗ_______________________£»
2)·“Ó¦¢ŪĄė×Ó·½³ĢŹ½___________________________________________________£»
3)·“Ó¦¢ßĄė×Ó·½³ĢŹ½___________________________________________________£»
4)·“Ó¦¢Ž»Æѧ·½³ĢŹ½___________________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖ³żČ„“ÖŃĪÖŠµÄCa2+”¢Mg2+”¢SO42-¼°ÄąÉ³£¬æɽ«“ÖŃĪČÜÓŚĖ®£¬Č»ŗó½ųŠŠĻĀĮŠĪåĻī²Ł×÷£ŗ¢Ł¹żĀĖ¢Ś¼Ó¹żĮæNaOHČÜŅŗ¢Ū¼ÓŹŹĮæŃĪĖį¢Ü¼Ó¹żĮæNa2CO3ČÜŅŗ¢Ż¼Ó¹żĮæBaCl2ČÜŅŗ”£ÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ £Ø £©
A. ¢Ś¢Ł¢Ü¢Ż¢Ū B. ¢Ś¢Ż¢Ü¢Ł¢Ū C. ¢Ü¢Ł¢Ś¢Ż¢Ū D. ¢Ł¢Ś¢Ü¢Ż¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĢžµÄ·Ö×ÓŹ½ĪŖC10H14 £¬ Ėü²»ÄÜŹ¹äåĖ®ĶŹÉ«£¬µ«æÉŹ¹KMnO4ĖįŠŌČÜŅŗĶŹÉ«£¬·Ö×Ó½į¹¹ÖŠÖ»ŗ¬ÓŠŅ»øöĶ黳£¬·ūŗĻĢõ¼žµÄĢžÓŠ£Ø £©
A.2ÖÖ
B.3ÖÖ
C.4ÖÖ
D.5ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÅēČŖŹĒŅ»ÖÖ³£¼ūµÄĻÖĻó£¬Ęä²śÉśŌŅņŹĒ“ęŌŚŃ¹Ēæ²ī”£ĻĀĆęŹĒijĶ¬Ń§Éč¼ĘµÄĖÄøö²»Ķ¬µÄÅēČŖ×°ÖĆ£¬ŌņŅŌĻĀĖµ·Ø²»ÕżČ·µÄŹĒ
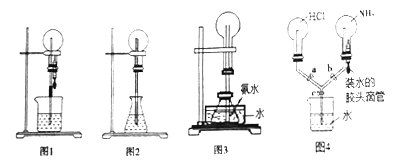
A. ČōĻņĶ¼1ÉÕĘæÖŠ³äĀśHI(ÓėHClĖ®ČÜŠŌĻąĖĘ)ĘųĢ壬ÉÕ±ÖŠ¼ÓČėAgNO3ČÜŅŗ£¬ŌņæÉŅŌ²śÉś»ĘÉ«ÅēČŖ
B. ČōĻņĶ¼2׶ŠĪĘæÖŠ¼ÓĖ®£¬ÉÕĘæÖŠ³äĀśSO2£¬Ņż·¢ÅēČŖµÄ²Ł×÷ŹĒĪęČČÉĻ·½µÄŌ²µ×ÉÕĘæ
C. ČōĻņĶ¼3×°ÖƵÄĖ®²ŪÖŠ¼ÓČė±łæé»ņĀżĀżµĪČėÅØĮņĖį¶¼æÉŅŌŠĪ³ÉÅēČŖ
D. Ķ¼4ĖłŹ¾µÄ×°ÖĆ£¬ČōŅŖŌŚøĆ×°ÖĆÖŠ²śÉśĖ«ÅēĻÖĻó£¬Ęä²Ł×÷·½·ØæÉŅŌŹĒ¹Ų±Õ»īČūc,“ņæŖ»īČūa”¢b£¬ŌŁ¼·Ń¹½ŗĶ·µĪ¹Ü£¬µ±²śÉś“óĮæµÄ°×ŃĢ£¬ŌŁ“ņæŖ»īČūc
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĢāŅāĢīæÕ
£Ø1£©2SO2£Øg£©+O2£Øg£© ”÷ v 2 O 5 2SO3£Øg£©£»”÷H=©196.6KJ/mol£¬ŹĒÖʱøĮņĖįµÄÖŲŅŖ·“Ó¦£®ĻĀĮŠ¹ŲÓŚøĆ·“Ó¦µÄŠšŹöÕżČ·µÄŹĒ £® £ØĢī×ÖÄø£©
A.“߻ƼĮV2O5²»øıäøĆ·“Ó¦µÄÄę·“Ó¦ĖŁĀŹ
B.Ōö“ó·“Ó¦ĢåĻµµÄŃ¹Ē棬·“Ó¦ĖŁĀŹŅ»¶ØŌö“ó
C.øĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬½µµĶĪĀ¶Č½«Ėõ¶Ģ·“Ó¦“ļµ½Ę½ŗāµÄŹ±¼ä
D.ŌŚt1”¢t2Ź±æĢ£¬SO3£Øg£©µÄÅØ¶Č·Ö±šŹĒc1 £¬ c2 £¬ ŌņŹ±¼ä¼äøōt1”«t2ÄŚ£¬SO3£Øg£©Éś³ÉµÄĘ½¾łĖŁĀŹĪŖu= c 2 c 1 t 2 t 1
E.Ź¹ÓĆ“ß»Æ¼ĮV2O5ÄÜĢįøßSO2µÄ×Ŗ»ÆĀŹ
F.Ź¹ÓĆ“ß»Æ¼ĮV2O5»įøıäøĆ·“Ó¦µÄ”÷H
£Ø2£©ÅŠ¶ĻøĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ £®£ØĢī×ÖÄø£©
a£®SO2ŗĶSO3ÅضČĻąµČ
b£®SO2°Ł·Öŗ¬Įæ±£³Ö²»±ä
c£®ŌŚĢå»ż²»±äµÄČŻĘ÷ÖŠ£¬ĘųĢåµÄŃ¹Ēæ²»±ä
d£®SO3µÄÉś³ÉĖŁĀŹÓėSO2µÄĻūŗÄĖŁĀŹĻąµČ
e£®ŌŚĢå»ż²»±äµÄČŻĘ÷ÖŠ»ģŗĻĘųĢ壬µÄĆܶȱ£³Ö²»±ä
f£®SO2”¢O2”¢SO3µÄÅØ¶Č±Č±£³Ö²»±ä£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĢāŅāĢīæÕ£ŗ
£Ø1£©ŹµŹĀÖ¤Ć÷£¬ÄÜÉč¼Ę³ÉŌµē³ŲµÄ·“Ó¦Ķس£ŹĒ·ÅČČ·“Ó¦£¬ĻĀĮŠ»Æѧ·“Ó¦ŌŚĄķĀŪÉĻæÉŅŌÉč¼Ę³ÉŌµē³ŲµÄŹĒ £®
A.C£Øs£©+H2O£Øg£©=CO£Øg£©Ź®H2£Øg£©”÷H£¾O
B.NaOH£Øaq£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©”÷H£¼O
C.2H2£Øg£©+O2£Øg£©=2H2O£Øl£©”÷H£¼0
£Ø2£©ŅŌKOHČÜŅŗĪŖµē½āÖŹČÜŅŗ£¬ŅĄ¾ŻĖłŃ”·“Ó¦Éč¼ĘŅ»øöŌµē³Ų£¬Ęäøŗ¼«·“Ó¦ĪŖ£ŗ £®
£Ø3£©µē½āŌĄķŌŚ»Æѧ¹¤ŅµÖŠÓŠ×Źć·ŗµÄÓ¦ÓĆ£®ĻÖ½«ÄćÉč¼ĘµÄŌµē³ŲĶعżµ¼ĻßÓėÓŅĶ¼ÖŠµē½ā³ŲĻąĮ¬£¬ĘäÖŠ£¬aĪŖµē½āŅŗ£¬XŗĶYŹĒĮ½æéµē¼«°å£¬Ōņ£ŗ
¢ŁČōXŗĶY¾łĪŖ¶čŠŌµē¼«£¬aĪŖCuSO4ČÜŅŗ£¬Ōņµē½āŹ±µÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ £® ĶعżŅ»¶ĪŹ±¼äŗó£¬ĻņĖłµĆČÜŅŗÖŠ¼ÓČė0.2molCu0·ŪÄ©£¬Ē”ŗĆ»Öø“µē½āĒ°µÄÅضČŗĶpH£¬Ōņµē½ā¹ż³ĢÖŠ×ŖŅʵĵē×ÓµÄĪļÖŹµÄĮæĪŖ £®
¢ŚČōX”¢Y·Ö±šĪŖĢśŗĶĶ£¬aČŌĪŖCuSO4ČÜŅŗ£¬ŌņY¼«µÄµē¼«·“Ó¦Ź½ĪŖ £®
£Ø4£©0.2molµÄĘųĢ¬øßÄÜČ¼ĮĻŅŅÅšĶé£ØB2H6£©ŌŚŃõĘųÖŠČ¼ÉÕ£¬Éś³É¹ĢĢ¬µÄČżŃõ»Æ¶žÅšŗĶŅŗĢ¬Ė®£¬·Å³ö433kJČČĮ棬ĘäČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ £® 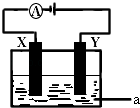
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÉÓĆĄ“¼ų±š¼ŗĻ©”¢¼×±½”¢ŅŅĖįŅŅõ„”¢±½·ÓČÜŅŗµÄŅ»×éŹŌ¼ĮŹĒ(””””)
A.FeCl3ČÜŅŗ”¢äåĖ®
B.Ģ¼ĖįÄĘČÜŅŗ”¢äåĖ®
C.ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ”¢äåĖ®
D.ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ”¢FeCl3ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚ1molL-1ĮņĖįČÜŅŗµÄĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A. 1LĖ®ÖŠŗ¬ÓŠ1mol H2SO4
B. 1LČÜŅŗÖŠŗ¬ÓŠ1mol H+
C. 1LĮņĖįČÜŅŗÖŠŗ¬ÓŠ96g SO42-
D. ½«98g H2SO4ČÜÓŚ1LĖ®ÖŠÅä³ÉÉĻŹöČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com