
用如图所示装置可以收集以下几种气体(烧瓶位置不动)(填字母,下同);
①H2 ②SO2 ③CH4④ HCl ⑤ NH3 ⑥ NO ⑦H2S
(1)若烧瓶是干燥的,则由A口进气,可收集到的气体有 ,由B口进气,可收集的气体有 。
(2)若在烧瓶中充满水,可收集的气体有 ,气体由 口进入。
(3)若此装置用于净化气体,在烧瓶内装有洗涤液,则混合气体应由 口进入。
(1)①③⑤;②④⑦ (2)①③⑥ A (3)B
解析试题分析:(1)关键装置图可知,若烧瓶是干燥的,由A口进气收集气体,这说明该气体的密度小于空气的,因此符合条件的是氢气、甲烷和氨气,答案选①③⑤;由B口进气收集气体,这说明该气体的密度大于空气的,因此符合条件的是SO2、氯化氢和H2S,NO极易被氧化,不能用排空气法收集,答案选②④⑦。
(2)若在烧瓶中充满水,收集气体,说明气体不溶于水,和水与不反应,则符合条件氢气、甲烷和NO,则答案选①③⑥,此时气体由A口进入。
(3)当烧瓶中装入洗液,用于洗气时,要使洗气更充分,则气体应从B口进入烧瓶。
考点:考查气体的收集以及洗气瓶的使用等
点评:该题是高考中的常见题型,属于中等难度试题的考查。试题针对性强,注重答题的灵活性,有利于培养学生的实验能力和实验分析和评价能力。注意收集气体时常根据气体的密度、溶解性等性质,有时还要考虑与氧气的反应等问题,如NO与氧气反应,则只能用排水法收集。
考点:
点评:


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
过氧化钙晶体[CaO2·8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
Ⅰ.过氧化钙晶体的制备。
工业上生产CaO2·8H2O的主要流程如下: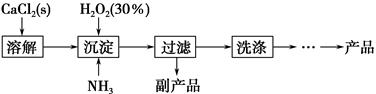
(1)用上述方法制取CaO2·8H2O的化学方程式是_________________________________。
(2)沉淀时常用冰水控制温度在10 ℃以下和通入过量的NH3,其可能原因分别是①__________________________;②_____________________________。
Ⅱ.过氧化钙晶体含量的测定。
准确称取0.300 0 g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1 H2SO4,用0.020 0 mol·L-1 KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
滴定终点观察到的现象为_______________________________________。
(4)根据表中数据,计算产品中CaO2·8H2O的质量分数(写出计算过程)。
KMnO4标准溶液滴定数据
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.300 0 | 1.02 | 24.04 |
| 2 | 0.300 0 | 2.00 | 25.03 |
| 3 | 0.300 0 | 0.20 | 23.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
为了提高资源利用率,减少环境污染,化工集团将钛厂、氯碱厂和甲醇厂组成产业链,如下图所示。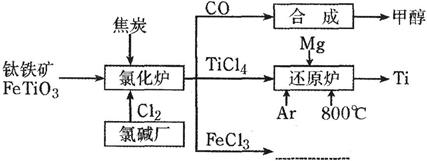
请填写下列空白:
(1)钛铁矿进入氯化炉前通常采取洗涤、粉碎、烘干、预热等物理方法处理,请从原理上解释粉碎的作用___________________;已知氯化炉中反应氯气和焦炭的理论用料物质的量比为7∶6,则氯化炉中的还原剂化学式是________________________;
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s) △H=-641kJ?molˉ1
② 2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s) △H=-512kJ?molˉ1
则Ti(s)+2Cl2(g)= TiCl4(s) △H= ;
(3)Ar气通入还原炉中并不参与反应,通入Ar气的作用是_______________________;
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH+3O2+4OHˉ=2CO32ˉ+6H2O,该电池中负极上的电极反应式是:2CH3OH-12eˉ+16OHˉ=2CO32ˉ+12H2O。则正极上发生的电极反应为:___________。工作一段时间后,测得溶液的pH是____(填“减小”、“增大”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铜是一种重要的金属元素,位于元素周期表第ⅠB族,+1价的铜与氯离子结合的生成的CuCl是一种难溶物质,但它可与过量的Cl-形成可溶于水的络离子[CuCl2]-。含铜最丰富的天然资源是黄铜矿(CuFeS2)。
(1)目前有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高。其主要流程如下:
①请完成反应Ⅰ中FeCl3与CuFeS2反应的化学方程式:
CuFeS2 + FeCl3 = +4 + 2S。
②写出反应Ⅳ中发生反应的离子方程式:
。
③反应Ⅲ是FeCO3在空气中煅烧,其化学方程式是
。
④已知Cu+在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu。则反应Ⅴ所得溶液A中含有的溶质有 。
(2)传统工艺从黄铜矿冶炼粗铜的技术,是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。与上面湿法冶炼技术方法比较,新方法的优点是 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
硫酸亚锡(SnSO4)、四氯化锡(SnCl4)常用于印染和电镀工业。
(1)某研究小组设计SnSO4制备路线如下:
已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化;SnCl2极易水解。
①SnCl2酸溶后加入Sn粉的作用是 ;
②步骤Ⅱ中用到的玻璃仪器除烧杯外还有 ;步骤Ⅳ中需要洗涤固体SnO中含有的杂质,检验SnO中的Cl-是否洗涤干净的操作为 。
③步骤Ⅴ涉及到的操作有:a.过滤 b.洗涤 c.蒸发浓缩 d.冷却结晶 e.低温干燥,则其正确的操作顺序为 。
(2)实验室拟用以下装置,用熔融的金属锡与干燥纯净的氯气制取无水SnCl4(SnCl4熔点-33℃,沸点114.1℃,遇潮湿空气极易水解),此反应过程放出大量的热。
①装置C中应加入试剂为 ;仪器E的名称为 。
②反应开始生成SnCl4时,可以先熄灭 (填字母序号)处的酒精灯,理由是 。
③该实验装置设计尚存在缺陷,改进的方法是(包括仪器、试剂及连接位置等) 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
过二硫酸钾(K2S2O8)是一种无色结晶,不溶于乙醇,有强氧化性,易分解。实验室制备过二硫酸钾可通过低温电解KHSO4认溶液得到。
实验步骤如下:
步骤1.称取40gKHSO4溶解90mL蒸馏水,倒入大试管,试管浸在冰水浴中(装置见图9),并冷却到5℃以下。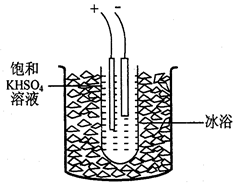
步骤2电解2h,每隔约半小时补一次冰
步骤3.将沉淀收集在漏斗中,直接用乙醇和乙醚洗涤和过滤
步骤4.干燥、称重
步骤5.回收乙醚和乙醇
(1)电解总反应的化学方程式为 。
(2)电解过程中,阳极产生微量且能使湿润的KI-淀粉变蓝的有色单质气体,该气体可能是(填化学式)。
(3)步骤2每隔半小时要向大烧杯添加冰块,其原因是 。
(4)步骤5回收乙醇、乙醚时采用的操作方法是 。
(5)取得到的样品0.2500g溶于30mL水,加4gKI,塞住瓶塞,振荡,静止15min,加入1mL冰醋酸,再用cmol·L- 1Na2S2O3溶液滴定。(S2O82- +3I- =2SO42- +I3-;I3- I2+I-;2S2O32-+I2=2I- + S4O62-)
I2+I-;2S2O32-+I2=2I- + S4O62-)
①溶解时,加入KI后需塞住瓶塞,其目的是 。
②本实验所用的指示剂为 。
③若本次滴定消耗Na2SO3溶液VmL,由本次结果计算,样品中K2S2O8的纯度为(用含c、V的代数式表示)。
(6)分析化学上检验Mn2+在Ag+催化下K2S2O8溶液将Mn2+氧化为紫色的MnO4-,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(本题16分)Ⅰ.实验室经常要制取某种气体并验证该气体的性质。
(1)下列装置适合作尾气吸收的是 (填序号)。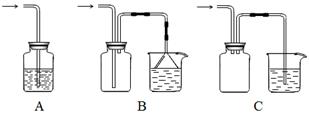
(2)向下列装置中通入气体X,A中品红溶液褪色,则X可能是___________(至少填两种)如果要证明X是SO2气体,接下来的操作是:________________________________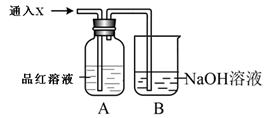
Ⅱ.实验室用FeSO4溶液和NaOH溶液反应制取Fe(OH)2,却很难看到稳定的白色沉淀。有同学设计了一种新的实验方法,能清楚看到生成白色沉淀及白色沉淀转化成红褐色沉淀的现象。请完成以下空白:
(1)取一定体积的0.1mol.L-1NaOH溶液放于烧杯中,_________后,再滴入几滴植物油;
(2)选择装置___________(填“甲”或“乙”),将(1)所得溶液加入到装置中并按图示组装好装置。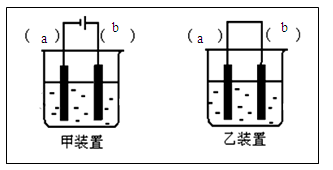
(3)在你选择的装置上标明电极材料分别为____________、________________
(4)实验中可在___________看到稳定的白色Fe(OH)2沉淀。
(5)如果要看到白色沉淀转化为红褐色沉淀的的现象,接下来的操作是______________
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(12 分)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
(1)一定条件下,NO 与NO2存在下列反应:NO(g)+NO2(g) N2O3(g),其平衡常数表达式为K = 。
N2O3(g),其平衡常数表达式为K = 。
(2)上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋), 其目的是 ;滤渣可循环使用,滤渣的主要成分是 (填化学式)。
(3)该工艺需控制NO 和NO2物质的量之比接近1 颐1。若n(NO):n(NO2)>1 颐1,则会导致 ;若n(NO):n(NO2)<1 颐1,则会导致 。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com