
����Ŀ��ij�����A������KAl(SO4)2��Al2O3��Fe2O3����һ�������¿�ʵ����ͼ��ʾ������֮��ı仯��
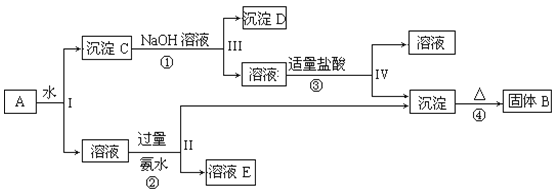
�ݴ˻ش��������⣺
��1��I��II��III��IV�IJ��ж�����Һ�ͳ����ķ����ȡ�ķ�����___��
��2������������ͼ��Ӧ��ϵ��д������B��C��D��E�������ʵĻ�ѧʽ��
����B___��C__������D___��
��3��д���١��ڡ��۵����ӷ���ʽ�ܵ͢Ļ�ѧ����ʽ��
��___��
��___��
��___��
��____��
���𰸡����� Al2O3 Al2O3��Fe2O3 Fe2O3 Al2O3+2OH-=2AlO2-+ H2O Al3++3NH3H2O=Al(OH)3��+3NH4+ AlO2-+ H2O+H+=Al(OH)3�� 2Al(OH)3 ![]() Al2O3+3H2O
Al2O3+3H2O
��������
�����A�к���KAl��SO4��2��Al2O3��Fe2O3����ˮ�ܽ��KAl(SO4)2����ˮ�γ���Һ��Al2O3��Fe2O3��������ˮ���γɳ���C������C�м�������������Һ��Fe2O3��������NaOH�У���˳���DΪFe2O3��Al2O3��ȫ�ܽ���NaOH�У��γ�NaAlO2�� NaAlO2��Һ�м������������ᣬ���γ�Al(OH)3���������Ⱥ�����Al2O3����KAl(SO4)2����ˮ�γɵ���Һ�м�������İ�ˮ���γ���Al(OH)3�����ͺ�NH4+��K+��SO42-����ҺE���ݴ˷�������
��1����Һ�ͳ����ķ���Ϊ��Һ���룬ͨ�����ù��˵ķ�����
��2���ɷ�����֪��BΪAl2O3��CΪAl2O3��Fe2O3��DΪFe2O3��
��3���ٷ�Ӧ��ΪAl2O3��NaOH��Һ�ķ�Ӧ��������ƫ�����ƺ�ˮ�����ӷ���ʽΪ��Al2O3+2OH-=2AlO2-+ H2O��
�ڷ�Ӧ��ΪAl3+������İ�ˮ֮��ķ�Ӧ�����ӷ���ʽΪ��Al3++3NH3H2O=Al(OH)3��+3NH4+��
�۷�Ӧ��ΪAlO2-��H+�ķ�Ӧ�����ӷ���ʽΪ��AlO2-+ H2O+H+=Al(OH)3����
�ܷ�Ӧ��ΪAl(OH)3���ȷֽ�ķ�Ӧ������ʽΪ��2Al(OH)3 ![]() Al2O3+3H2O��
Al2O3+3H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤����ʵ�����Ʊ��õ���Cl2�л����HCl����ͬѧ�������ͼ��ʾ��ʵ��װ�ã���Ҫ��ش��������⡣
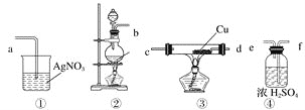
��1������ݼ�ͬѧ��ʾ��ͼ������ʵ��װ�ô������ҵ�����˳��װ�â���__________��
��2��װ�â�����Ҫ��������������__________��__________��__________��
��3��ʵ�����Ʊ�Cl2�����ӷ���ʽΪ____________��
��4��װ�â���Cu������__________���û�ѧ����ʽ��ʾ����
��5����ͬѧ��Ϊ��ͬѧʵ�������Ȼ����ȱ�ݣ�����֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�Ϊ�ˣ���ͬѧ�������ͨ��װ�â�֮ǰ��Ҫ��װһ������װ�âݣ���֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�����Ϊװ�â�Ӧ����__________��
��6����ͬѧ������ͬѧ��Ƶ�װ�ú����������װ�ã�ֻ�轫ԭ���ձ��е�AgNO3��Һ������ɫʯ����Һ������۲쵽__________��������֤����Cl2ʱ��HCl�ӷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A.1.8 g NH4�����еĵ�����ΪNA
B.1 L 1 mol��L��1��NaAlO2ˮ��Һ�к��е���ԭ����Ϊ2NA
C.����£�22.4 L NO��11.2 L O2��ַ�Ӧ��������ķ�������ΪNA
D.50 mL 18 mol��L��1��Ũ������������ͭƬ���ȣ�����SO2�ķ�����Ϊ0.45NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ָ�������������ϵı���ͨ�����û��������ɵĶ�л�����������ij����������������졢�ơ��ŵȣ���ṹ�ֱ�Ϊ
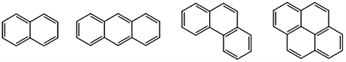
�� �� �� ��
����˵������ȷ����
A. ���ķ���ʽΪC10H8����H2��ȫ�ӳɺ���ķ���ʽΪC10H18
B. �졢�ơ��ŵ�һ�ȴ���ֱ���3�֡�5�֡�5��
C. �����������ʵķ����У�����̼ԭ�Ӿ���ƽ��
D. �����������ʾ�����Ũ���ᷢ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�¶�ʱ��nmol��L-1��ˮ����10mLymol��L-1�����У���ҺpH���¶�����백ˮ����仯������ͼ��ʾ�������й�˵������ȷ���ǣ� ��
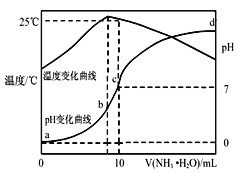
A.y=1.0
B.a��ʱKw<1��10-14
C.b��c(NH4+)<c(Cl-)=![]() mol��L-1
mol��L-1
D.25��ʱ��NH4Cl��ˮ�ⳣ��(Kh)�ɱ�ʾΪ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���ѧ����ʽ��д��ȷ���ǣ� ��
A. CH4��Cl2![]() CH2Cl2��H2
CH2Cl2��H2
B. H2C=CH2��Br2��CH3CHBr2
C. 2CH3CH2OH��O2![]() 2CH3CHO��2H2O
2CH3CHO��2H2O
D. CH3CH2OH��CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����̽��SO2���ʵ�װ����ͼ��ʾ������˵��������ǣ� ��
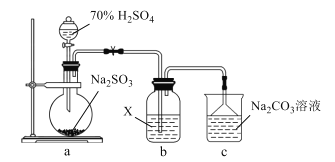
A.װ��a�еķ�Ӧ����ͭƬ��Ũ�������
B.��XΪH2S��Һ��װ��b�в�������ɫ����
C.��XΪ��HCl��BaCl2��FeCl3��Һ��װ��b�в�����ɫ����
D.��Ӧ��װ��c����Һ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������V2O5Ϊԭ���Ʊ�����(��)��ʽ̼��茶���{(NH4)5[(VO)6(CO3)4(OH)9]��10H2O}�����������£�
V2O5![]() VOCl2��Һ
VOCl2��Һ![]() ����(��)��ʽ̼��茶���
����(��)��ʽ̼��茶���
(1)����ԭ�������еĻ�ԭ����____________(�ѧʽ)��
(2)��֪VO2+�ܱ�O2��������ת����������ͼװ���н��С�
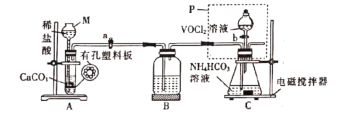
������M��������___________��ʵ�鿪ʼǰ�IJ�����_________��
��װ��B��������__________________��
�ۼ���VOCl2��Һ���������һ��ʱ�䣬ʹ��Ӧ��ȫ���ٽ������в�����˳��Ϊ_______(����ĸ)��
a.��ƿ����������
b.ȡ��P
c.����ƿ���ڸ������У����ù�ҹ
�ܵõ��Ϻ�ɫ���壬���ˣ����ñ���NH4HCO3��Һϴ��3�Σ�����ˮ�Ҵ�ϴ��2�Σ���������ϴ��2�Σ���ɳ��ء��ñ���NH4HCO3��Һϴ�ӳ�ȥ����������Ҫ��_______(�����ӷ���)������ˮ�Ҵ�ϴ�ӵ�Ŀ����_______________��
�ݳ���![]() ��Ʒ����ƿ�У���20mL����ˮ��30mLϡ�����ܽ����0.02mol/L KMnO4��Һ���Թ�������ַ�Ӧ������μ�1%��NaNO2��Һ���Թ������������س�ȥ����NaNO2�������c mol/L (NH4)2Fe(SO4)2����Һ�ζ����յ�(��֪�ζ���ӦΪ
��Ʒ����ƿ�У���20mL����ˮ��30mLϡ�����ܽ����0.02mol/L KMnO4��Һ���Թ�������ַ�Ӧ������μ�1%��NaNO2��Һ���Թ������������س�ȥ����NaNO2�������c mol/L (NH4)2Fe(SO4)2����Һ�ζ����յ�(��֪�ζ���ӦΪ![]() +Fe2++2H+=VO2++Fe3++H2O)�����ı���Һ�����ΪV mL����(NH4)2Fe(SO4)2����Һ���ֱ��ʣ���ʹ�ⶨ���______________(����ƫ������ƫ����������Ӱ����)����Ʒ�з�����������Ϊ_________(��VO2+�������м��㣬�г�����ʽ)��
+Fe2++2H+=VO2++Fe3++H2O)�����ı���Һ�����ΪV mL����(NH4)2Fe(SO4)2����Һ���ֱ��ʣ���ʹ�ⶨ���______________(����ƫ������ƫ����������Ӱ����)����Ʒ�з�����������Ϊ_________(��VO2+�������м��㣬�г�����ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Aת��ΪC��D�ֲ����У���A(g)![]() B(g)+2D(g)��B(g)
B(g)+2D(g)��B(g)![]() C(g)+D(g)���䷴Ӧ����������ͼ��ʾ������˵����ȷ���ǣ� ��
C(g)+D(g)���䷴Ӧ����������ͼ��ʾ������˵����ȷ���ǣ� ��
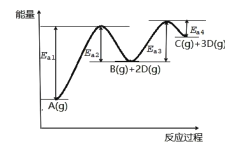
A.1molA(g)����������1molB(g)������
B.B(g)![]() C(g)+D(g) ��H=Ea4-Ea3
C(g)+D(g) ��H=Ea4-Ea3
C.����1molA(g)��ѧ�����յ�����С���γ�1molC(g)��3molD(g)��ѧ�����ų�������
D.��Ӧ�����У�����Ea3<Ea1����Ӧ�����ʴ��ڷ�Ӧ�٣�����B���Ѵ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com