
·ÖĪö £Ø1£©¢ŁÖ»ŅŖĖµĆ÷Ņ»Ė®ŗĻ°±ŌŚĖ®ČÜŅŗÖŠ²æ·ÖµēĄė¾ĶÄÜÖ¤Ć÷Ņ»Ė®ŗĻ°±ŹĒČõ¼ī£¬æÉŅŌøł¾ŻŅ»¶ØÅضČČÜŅŗµÄpH”¢ĒæĖįļ§ŃĪµÄĖį¼īŠŌµČ·ÖĪöÅŠ¶Ļ£»
¢ŚŹ¹°±Ė®µēĄė³Ģ¶ČŌö“󣬼ÓĖ®”¢¼ÓÓėļ§øłĄė×Ó»ņĒāŃõøłĄė×Ó·“Ó¦µÄĪļÖŹ”¢»ņÉżøßĪĀ¶Č£»
£Ø2£©¢Ł“×ĖįĪŖČõĖį£¬ŃĪĖįĪŖĒæĖį£¬µČÅØ¶ČŹ±“×ĖįµÄpH“ó£»
¢ŚĖįŗĶ¼ī¶¼¶ŌĖ®µÄµēĄėĘšŅÖÖĘ×÷ÓĆ£¬Ėį”¢¼īŠŌŌ½Ē棬Ė®µÄµēĄė³Ģ¶ČŌ½Š”£»
¢Ū“×ĖįÄĘĻŌŹ¾¼īŠŌ£¬ĀČ»ÆÄĘĻŌŹ¾ÖŠŠŌ£»
¢Ü0.1mol•L-1 NaOHČÜŅŗ10mLŗĶČÜŅŗĢå»żĪŖ20.00mL0.1mol•L-1µÄ“×Ėį·“Ó¦£¬µĆµ½µÄŹĒ“×ĖįŗĶ“×ĖįÄʵĻģŗĻĪļ£¬¾Ż“ĖČ·¶ØĄė×ÓÅØ¶Č“óŠ”£®
½ā“š ½ā£ŗ£Ø1£©¢ŁA£®°±Ė®ŗĶĀČ»ÆŃĒĢś·“Ӧɜ³ÉĒāŃõ»ÆŃĒĢś³Įµķ£¬ĖµĆ÷Ņ»Ė®ŗĻ°±ŹĒ¼ī£¬µ«²»ÄÜĖµĆ÷Ņ»Ė®ŗĻ°±²æ·ÖµēĄė£¬ĖłŅŌ²»ÄÜĖµĆ÷ŹĒČõµē½āÖŹ£¬¹ŹA“ķĪó£»
B£®³£ĪĀĻĀ£¬0.1mol•L-1°±Ė®pHĪŖ11£¬ČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷Ņ»Ė®ŗĻ°±²æ·ÖµēĄė£¬ŌņĖµĆ÷Ņ»Ė®ŗĻ°±ŹĒČõµē½āÖŹ£¬¹ŹBÕżČ·£»
C£®ļ§ŃĪŹÜČČŅ×·Ö½āĖµĆ÷ļ§ŃĪ²»ĪČ¶Ø£¬²»ÄÜĖµĆ÷Ņ»Ė®ŗĻ°±²æ·ÖµēĄė£¬Ōņ²»ÄÜĖµĆ÷Ņ»Ė®ŗĻ°±ŹĒČõµē½āÖŹ£¬¹ŹC“ķĪó£»
D£®³£ĪĀĻĀ£¬0.1mol/LµÄĀČ»Æļ§ČÜŅŗpHŌ¼ĪŖ5£¬ČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷ĀČ»Æļ§ŹĒĒæĖįČõ¼īŃĪ£¬ŌņĖµĆ÷Ņ»Ė®ŗĻ°±ŹĒČõµē½āÖŹ£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗBD£»
¢ŚA£®ĶØČė°±Ęų£¬°±Ė®µÄÅضČŌö“󣬵ēĄė³Ģ¶Č¼õŠ”£¬¹ŹA“ķĪó£»
B£®¼ÓČėÉŁĮæĀČ»ÆĢś¹ĢĢ壬»įĻūŗÄĒāŃõøłĄė×Ó£¬Ōņ“Ł½ųŅ»Ė®ŗĻ°±µÄµēĄė£¬µēĄė³Ģ¶ČŌö“󣬹ŹBÕżČ·£»
C£®¼ÓĖ®Ļ”ŹĶ£¬“Ł½ųŅ»Ė®ŗĻ°±µÄµēĄė£¬µēĄė³Ģ¶ČŌö“󣬹ŹCÕżČ·£»
D£®¼ÓČėÉŁĮæĀČ»Æļ§¹ĢĢ壬ļ§øłĄė×ÓÅضČŌö“ó£¬ŅÖÖĘ°±Ė®µÄµēĄė£¬µēĄė³Ģ¶Č¼õŠ”£¬¹ŹD“ķĪó£»
¹Ź“š°øĪŖ£ŗBC£»
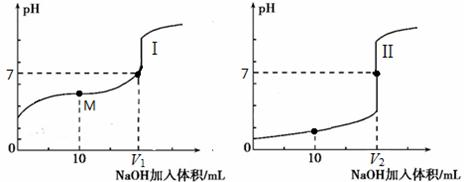
£Ø2£©¢ŁÓÉĶ¼ÖŠĪ“¼ÓNaOHŹ±µÄpHæÉÖŖ£¬Ķ¼¢ńÖŠĖįµÄpH“óÓŚ1£¬Ķ¼¢ņÖŠĖįµÄpH=1£¬ĖµĆ÷¢ņĪŖ0.1mol/LµÄŃĪĖįČÜŅŗ£¬ĪŖ“×ĖįČÜŅŗµĪ¶Ø¹ż³Ģ£¬ĖłŅŌµĪ¶Ø“×ĖįµÄĒśĻߏĒI£¬
¹Ź“š°øĪŖ£ŗI£»
¢Ś0.1mol•L-1 NaOHČÜŅŗ”¢0.1mol•L-1µÄŃĪĖįÖŠĒāĄė×ÓŗĶĒāŃõøłÅØ¶Č¶¼ŹĒ0.1mol/L£¬¶ŌĖ®µÄŅÖÖĘ×÷ÓĆŅ»Ńł£¬µ«ŹĒ0.1mol/L“×ĖįČÜŅŗÖŠĒāĄė×ÓÅØ¶ČŠ”ÓŚ0.1mol/L£¬ĖłŅŌ¶ŌĖ®µÄµēĄėŅÖÖĘ½ĻŠ”£¬¼“ČżÖÖČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØH+£©×ī“óµÄŹĒ0.1 mol•L-1“×ĖįČÜŅŗ£¬¹Ź“š°øĪŖ£ŗ0.1mol•L-1“×ĖįČÜŅŗ£»
¢Ū“×ĖįŗĶĒāŃõ»ÆÄĘÖ®¼äµÄ·“Ó¦£¬µ±Ē”ŗĆĶźČ«·“Ó¦µĆµ½µÄ“×ĖįÄĘĻŌŹ¾¼īŠŌ£¬ŅŖŹ¹µĆČÜŅŗĻŌŹ¾ÖŠŠŌ£¬pH=7£¬ŠčŅŖ“×ĖįÉŌ¹żĮ棬ĖłŅŌŃĪĖįŗĶĒāŃõ»ÆÄĘĒ”ŗĆĶźČ«·“Ó¦£¬µĆµ½µÄĀČ»ÆÄĘĻŌŹ¾ÖŠŠŌ£¬ĖłŅŌV1£¼V2£¬¹Ź“š°øĪŖ£ŗ£¼£»
¢ÜÓĆ0.1mol•L-1 NaOHČÜŅŗ10mLŗĶČÜŅŗĢå»żĪŖ20.00mL0.1mol•L-1µÄ“×Ėį·“Ó¦£¬µĆµ½µÄŹĒ“×ĖįŗĶ“×ĖįÄʵĻģŗĻĪļ£¬ĻŌŹ¾ĖįŠŌ£¬“ĖŹ±Ąė×ÓÅØ¶Č“óŠ”c£ØCH3COO-£©£¾c £ØNa+£©£¾c £ØH+£©£¾c £ØOH-£©£¬¹Ź“š°øĪŖ£ŗc£ØCH3COO-£©£¾c £ØNa+£©£¾c £ØH+£©£¾c £ØOH-£©£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éѧɜĖį¼īµĪ¶ØŅŌ¼°ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”±Č½ĻµÄÖŖŹ¶£¬ŹōÓŚ×ŪŗĻÖŖŹ¶µÄ漲飬Ķ¼Ļó·ÖĪöÅŠ¶ĻŹĒ½āĢā¹Ų¼ü£¬ÕĘĪÕ»ł“”ŹĒ¹Ų¼ü£¬ÄѶČÖŠµČ£®


 °ŁÄźŃ§µäæĪŹ±Ń§Į·²āĻµĮŠ“š°ø
°ŁÄźŃ§µäæĪŹ±Ń§Į·²āĻµĮŠ“š°ø ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆĪĀ¶ČĻĀ£¬0.0l mol/L“×ĖįČÜŅŗµÄpH=4 | |
| B£® | øĆĪĀ¶ČĻĀ£¬ÓĆ0.1 mol/L“×ĖįŗĶ0.01 mol/L“×Ėį·Ö±šĶźČ«ÖŠŗĶµČĢå»ż0.1 mol/LµÄNaOHČÜŅŗ£¬ĻūŗÄĮ½“×ĖįµÄĢå»ż±ČĪŖ1£ŗ10 | |
| C£® | øĆĪĀ¶ČĻĀ£¬0.2 mol/L“×ĖįČÜŅŗŗĶ0.4 mol/L“×ĖįÄĘČÜŅŗµČĢå»ż»ģŗĻŗ󣬻ģŗĻŅŗµÄpH£¼4.7 | |
| D£® | øĆĪĀ¶ČĻĀ£¬0.2 mol/LŃĪĖįČÜŅŗŗĶ0.4 mol/L“×ĖįÄĘČÜŅŗµČĢå»ż»ģŗĻŗ󣬻ģŗĻŅŗµÄpH£¾4.7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅ“¼ŗĶŅŅĖįÄÜ·¢Éśõ„»Æ·“Ó¦£¬Ö»ŅŖŅ»ÖÖ·“Ó¦Īļ¹żĮæõ„»Æ·“Ó¦¾ĶÄܽųŠŠ³¹µ× | |
| B£® | °ŃŅŅĻ©ĶØČėäåĖ®ÖŠ£¬äåĖ®Į¢¼“ĶŹÉ«£¬ÕāŹĒÓÉÓŚŅŅĻ©¾ßÓŠĘư׊Ō | |
| C£® | ĆŗµÄĘų»ÆŗĶĆŗµÄøÉĮ󶼷¢ÉśĮĖ»Æѧ±ä»Æ£¬¶ųŹÆÓĶµÄ·ÖĮóŹōÓŚĪļĄķ±ä»Æ | |
| D£® | ±½²»ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬Ņņ“Ė±½²»ÄÜ·¢ÉśŃõ»Æ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ü | B£® | ¢Ł¢Ś¢Ü | C£® | ¢Ś¢Ū | D£® | ¢Ł¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ĶéµÄČ¼ÉÕČČĪŖ890.3 kJ•mol-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖCH4£Øg£©+2O2£Øg£©=CO2£Øg£©+2H2O£Øg£©”÷H=-890.3 kJ•mol-1 | |
| B£® | 101 kPaŹ±£¬2 g H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®·Å³ö285.8 kJČČĮ棬ĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ2H2£Øg£©+O2£Øg£©=2H2O£Øl£©”÷H=-571.6 kJ•mol-1 | |
| C£® | HClŗĶNaOH·“Ó¦µÄÖŠŗĶČČ”÷H=-57.3 kJ•mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø-57.3£©kJ•mol-1 | |
| D£® | 500”ę”¢30 MPaĻĀ£¬½«0.5 mol N2£Øg£©ŗĶ1.5 mol H2£Øg£©ÖĆÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³ÉNH3£Øg£©·ÅČČ19.3 kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-38.6 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| W | X | |
| Y | Z |
| A£® | X”¢Y”¢ZČżÖÖŌŖĖŲµÄ×ī¼ņµ„Ēā»ÆĪļÖŠ×ī²»ĪČ¶ØµÄŹĒY | |
| B£® | W”¢Y”¢ZČżÖÖŌŖĖŲ¶ŌÓ¦Ńõ»ÆĪļµÄĖ®»ÆĪļŅ»¶Ø¶¼ŹĒĒæĖį | |
| C£® | W”¢XŌŖĖŲµÄ×ī¼ņµ„Ēā»ÆĪļ¶¼ŹĒ·Ēµē½āÖŹ | |
| D£® | ZŌŖĖŲµÄµ„ÖŹŌŚ»Æѧ·“Ó¦ÖŠÖ»ÄܱķĻÖŃõ»ÆŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŌŖĖŲ±ąŗÅ | ŌŖĖŲŠŌÖŹ»ņŌ×Ó½į¹¹ |
| T | M²ćµē×ÓŹżŹĒK²ćµē×ÓŹżµÄ3±¶ |
| X | Ņ»ÖÖĶ¬Ī»ĖŲæɲā¶ØĪÄĪļÄź“ś |
| Y | ³£ĪĀĻĀµ„ÖŹĪŖĖ«Ō×Ó·Ö×Ó£¬ĘäĒā»ÆĪļĖ®ČÜŅŗ³Ź¼īŠŌ |
| Z | ŌŖĖŲ×īøßÕż¼ŪŹĒ+7¼Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Sn£ØNO3£©4 | B£® | Sn£ØNO3£©2 | C£® | SnO2?4H2O | D£® | SnO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOHæÉÓĆÓŚÖĪĮĘĪøĖį¹ż¶ą | |
| B£® | CaOæÉ·ĄÖ¹ŌĀ±żµČŹ³Ę·Ńõ»Æ±äÖŹ | |
| C£® | ĒāµÆÖŠÓƵ½µÄ2H”¢3H»„ĪŖĶ¬Ī»ĖŲ | |
| D£® | Ļņŗ£Ė®ÖŠ¼ÓČė¾»Ė®¼ĮĆ÷·ÆæÉŅŌŹ¹ŗ£Ė®µ»Æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com