
参考下列图表和有关要求回答问题。
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中能量变化示意图,若
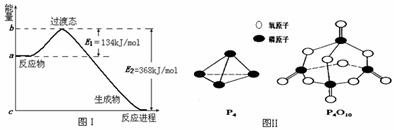
在反应体系中加入催化剂,反应速率增大,E1的变化是______,△H的变化是___________(填“增大”、“减小”、“不变”)。请写出NO2和CO反应的热化学方程式: ;
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是: ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H= + 49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ·mol-1
又知 ③H2O(g)= H2O(l) △H=-44 kJ/mol
则甲醇燃烧的热化学方程式为 ;
(3)下表是部分化学键的键能数据:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/ kJ·mol–1 | a | b | c | x |
已知白磷的燃烧热为d kJ·mol–1,白磷及其完全燃烧的产物结构如图Ⅱ所示,则上表中x=________________kJ·mol–1(用含有a、b、c、d的代数式表示)
科目:高中化学 来源: 题型:
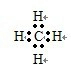
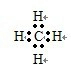
 ; ⑧
; ⑧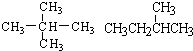 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
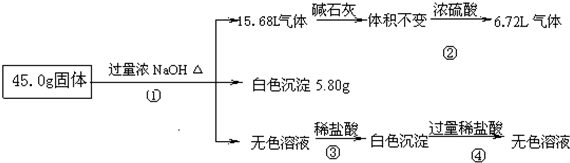
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
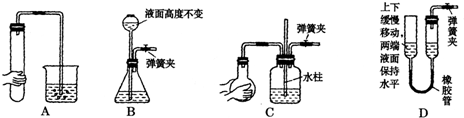
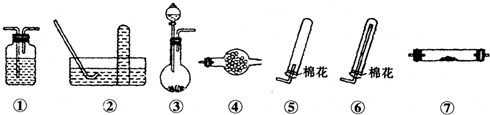
| 物质 | 熔点/℃ | 沸点℃ | 化学性质 | ||||
| S | 112.8 | 444.6 | 略 | ||||
| S2Cl2 | -77 | 137 | 遇水生成HCl,SO2,S;300℃以上完全分解; S2Cl2+Cl2
|
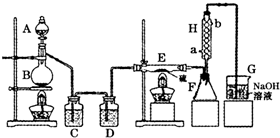
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:河南省模拟题 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com