
高纯硅生产流程如下: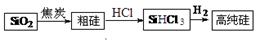
(1)由SiO2制粗硅的化学方程式是 ,该反应不能说明碳的非金属性强于硅,原因是 ,请写出一个能说明碳的非金属性强于硅的化学方程式 。
(2)900℃以上,H2与SiHCl3发生反应:SiHCl3(g)+ H2(g) Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是 (填字母)。
Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是 (填字母)。
a.在恒温条件下,若容器内压强不变,则该反应一定达到化学平衡状态
b.增大SiHCl3的用量,可提高SiHCl3的平衡转化率
c.升高温度可加快反应速率,且提高硅的产率
(3)该流程中可以循环使用的物质是 。
(1)SiO2+2C Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+2H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3。
Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+2H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3。
(2)a c (3)HCl、H2
解析试题分析:(1)SiO2+2C Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+3H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3
Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+3H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3
(2)从化学方程式来看,气体反应物和气体生成物的化学计量数不相等,即是一个气体体积在反应前后存在变化的化学反应,压强在反应过程中也存在变化,当不再变化时,说明达到平衡,a正确;增大SiHCl3的用量,可提高H2的平衡转化率,SiHCl3的平衡转化率反而减小。b错误;该反应正反应方向是吸热反应,升高温度向着吸热反应的方进行,平衡右移,c正确。(3)HCl、H2
考点:考查硅及其化合物的性质、化学方程式的属性、非金属性的强弱比较方法、化学平衡。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_____________。
(2)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:_______________________________________。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO。原因是_______________,
元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
把19.2 g 的Cu放入500mL 2 mol·L-1稀硝酸中,充分反应,Cu完全溶解。求:
(1)写出Cu与稀硝酸反应的离子方程式: ;
(2)铜完全溶解时转移电子数目为 (用含NA的式子表示);
(3)氧化剂与还原剂的物质的量比为 。
(4)反应后溶液中C(H+)为 (体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)某化学兴趣小组的同学进行Cl2、NH3的制备及性质检验等实验的流程和部分装置如下:
请利用A、G装置设计一个简单的实验验证Cl2、Fe3+、I2的氧化性强弱为Cl2>Fe3+>I2(实验中不断地小心振荡G装置中的试管)。A中反应物是KMnO4和浓盐酸,请写出A中发生反应的化学方程式: ,请写出试剂M为 溶液,证明氧化性为Cl2>Fe3+>I2的实验现象是 。
②已知3Cl2+2NH3=6HCl+N2,当D的烧瓶中充满黄绿色气体后,关闭a、c打开b,D中的现象为黄绿色气体消失,产生白烟,反应一段时间后,关闭b打开c,观察到的现象为_________________________________________________________________。
(2)某废水中含有一定量的Na+、SO ,可能含有CO
,可能含有CO ,某研究小组欲测定其中SO
,某研究小组欲测定其中SO 的浓度,设计如下实验方案:
的浓度,设计如下实验方案:
①从下列试剂中选择试剂X为_________(填序号);
A.0.1 mol/L KMnO4(H2SO4酸化)溶液 B.0.5 mol/L NaOH溶液
C.新制氯水 D.KI溶液
②加入试剂X生成SO 的离子方程式为_____________________________________;
的离子方程式为_____________________________________;
③证明该废水中是否含有CO 的实验方案为 。
的实验方案为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
固体硝酸盐加热易分解且产物较复杂。已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐的热分解反应方程式如下:
I.2KNO3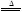 2KNO2+O2↑
2KNO2+O2↑
II.2Cu(NO3) 2 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
III.2AgNO3 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
(1)某固体可能由KNO3、Cu(NO3)2、AgNO3三种硝酸盐中的一种或几种组成。取适量该固体充分加热,得到一定量气体。若该气体经水充分吸收后,剩余气体的体积在同温同压下为吸收前的1/6。 (忽略氧在水中的溶解)
①若该固体只是由一种盐组成,则该盐为 。
②若该固体是混合物,则该混合物的可能组成为 。
(2)某学习小组以Mg(NO3)2为研究对象,通过实验探究其热分解的产物,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):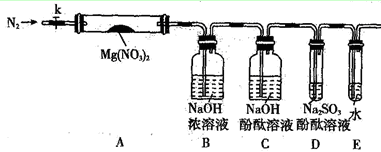
【实验步骤】
a.仪器连接后,放入固体试剂之前,关闭k,微热硬质玻璃管A。
b.称取Mg(NO3)2固体3.7g置于A中,先通入一段时间N2,再关闭k,用酒精灯加热硬质玻璃管A。
c.待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g。
①步骤a的目的是 ;
②依据已知的三个方程式,再根据剩余固体的质量写出Mg(NO3)2热分解方程式为: 。
③若A中固体为AgNO3,用以上实验装置进行实验时,D 中的现象为 ,用离子方程式表示出现该现象的原因:_____________________ 。
④从实验安全的角度判断该实验装置有无缺陷?若有,应如何改进? 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氯气在298K、100kPa时,在1L水中可溶解0.090mol,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
(1)该反应的离子方程式为____________________________;
(2)根据离子方程式,计算该反应的平衡常数(水视为纯液体,列式计算,保留2位有效数字)
(3)在上述平衡体系中加入少量NaOH固体,平衡将向________移动;(填“正”、“逆”或“不”)
(4)如果增大氯气的压强,氯气在水中的溶解度将______(填“增大”、“减小”或“不变”),平衡将向______________移动。(填“正”、“逆”或“不”)
(5)新制氯水经光照一段时间后溶液c(H+)增大,请运用平衡移动原理进行解释:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有X、Y、Z三种元素,已知:①X、Y、Z的单质在常温下均为气体;②X单质可在Z单质中燃烧,生成气态XZ;③XZ极易溶于水,电离出X+和Z-,其水溶液可使蓝色石蕊试纸变红;④每2个X2分子可与1个Y2分子化合生成2个X2Y分子,X2Y在常温下为无色液体;⑤Z单质溶于X2Y中,所得溶液具有漂白作用。
(1)推断X,Y两种元素:X________,Y_________(填元素名称)。
(2)写出⑤过程中的化学反应的方程式 。
(3)写出工业上制取Z单质的化学方程式 。
(4)写Z单质与石灰乳反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
(1)N2H4中的N原子可达到8电子的稳定结构,画出N2H4的结构式_____________。
(2)实验室用两种固体制取NH3的反应方程式为______________________________。
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 。
(4)肼——空气燃料电池是一种碱性电池,该电池放电时,负极的反应式 。
(5)肼是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942,O=O为500,N-N为154,则断裂1molN-H键所需的能量是 kJ。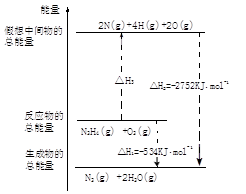
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(16)某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。其实验流程图如下:
(1)测定硝酸的物质的量反应结束后,从下图B装置中所得100mL溶液中取出25.00mL溶液,用0.1mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如右上图所示。在B容器中生成硝酸的物质的量为 mol。
(2)测定NO的体积
①从上图所示的装置中,你认为应选用 装置进行Cu与浓硝酸反应实验,选用的理由是 。
②选用上图所示仪器组合一套可用来完成实验并测定生成NO体积的装置,其合理的连接顺序是(填各导管口编号) 。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置 (“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
(3)气体成分分析:若实验测得NO的体积为112.0mL(已折算到标准状况),则Cu与浓硝酸反应的过程中 (填“有”或“没有”)NO产生,作此判断的依据是 。
(4)实验前,用托盘天平称取的铜片至少应为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com