
| A. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| B. | 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 | |
| C. | 铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| D. | 用含有橙色的酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的氧化性 |
分析 A.同分异构体:分子式相同结构不同的化合物;
B.硫、氮的氧化物溶于水生成酸;
C.Fe在潮湿的空气中易发生电化学腐蚀;
D.酸性重铬酸钾溶液具有强氧化性.
解答 解:A.棉和麻主要成分是纤维素,与淀粉分子中的n值不同,不属于同分异构体,故A错误;
B.硫、氮的氧化物溶于水生成酸,减少硫、氮的氧化物的排放可以减少酸雨产生,所以燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施,故B正确;
C.Fe在潮湿的空气中,Fe、C和电解质溶液易构成原电池,Fe作负极被腐蚀,发生电化学腐蚀,故C错误;
D.酸性重铬酸钾溶液具有强氧化性,酸性重铬酸钾与乙醇反应时乙醇作还原剂,酸性重铬酸钾作氧化剂,故D错误.
故选B.
点评 本题考查了同分异构体、环境保护、金属的腐蚀、氧化还原反应,题目难度不大,旨在考查学生对基础知识的识记,注意基础知识的积累掌握,注意化学知识在生产生活中的应用.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:解答题
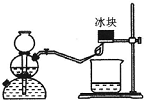 (1)下面所列的是中学化学实验室中几种常见的仪器:容量瓶、酸式滴定管、碱式滴定管、温度计、量筒、托盘天平、普通漏斗、玻璃棒、烧杯.
(1)下面所列的是中学化学实验室中几种常见的仪器:容量瓶、酸式滴定管、碱式滴定管、温度计、量筒、托盘天平、普通漏斗、玻璃棒、烧杯.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
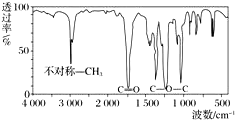 取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )
取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )| A. | 其化学式为C4H8O2 | |
| B. | 其满足右侧图象的酯有3种 | |
| C. | 鉴定该有机物的结构可用红外光谱或核磁共振氢谱 | |
| D. | 若结构为CH3COOCH2CH3,其核磁共振氢谱中有3个峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe( NO3)3溶液中加入过量HI溶液:2Fe3++2I-═2Fe2++I2 | |
| B. | 浓烧碱溶液中加入铝片:2A1+2OH-═2AlO2-+H2 | |
| C. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4+H2O | |
| D. | 将新制氢氧化铜悬浊液加入氨水中:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++2OH-+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +352 | B. | +132 | C. | -120 | D. | -330 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成原电池正极和负极的材料必须是两种金属 | |
| B. | 由铜、锌电极与硫酸铜溶液组成的原电池铜是负极 | |
| C. | 电子沿导线由锌流向铜,通过硫酸溶液被氢离子得到而放出氢气 | |
| D. | 铜锌原电池工作时,锌被硫酸溶解,所以才产生电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释时溶液中各离子浓度均减小 | |
| B. | 加强酸弱酸强碱弱碱均抑制盐类的水解 | |
| C. | 正盐水溶液的pH均为7 | |
| D. | 酸式盐的pH均小于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C9H10O2 | B. | C9H12O2 | C. | C9H16O2 | D. | C9H18O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com