



 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 序号 | 实验现象 | 结 论 |
| A | 热水中平衡球颜色比冷水中深 | 升温,化学平衡向吸热反应方向移动 |
| B | 起始时产生气泡速率HCl>CH3COOH | 醋酸是弱电解质 |
| C | 溶液颜色由黄变橙,且30秒内不变色 | 已达滴定终点 |
| D | 划口处有蓝色沉淀 | 铁发生了析氢腐蚀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
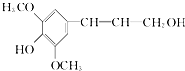
| A、芥子醇的分子式是C11H14O4,属于芳香烃 |
| B、芥子醇分子中所有碳原子不可能在同一平面上 |
| C、芥子醇与足量浓溴水反应,最多消耗1 mol Br2 |
| D、芥子醇能发生的反应类型有氧化、取代、加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、K+、Cl-、NO3- |
| B、H+、K+、HCO3-、NO3- |
| C、Cu2+、NO3-、SO42-、Cl- |
| D、OH-、Cl-、Na+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

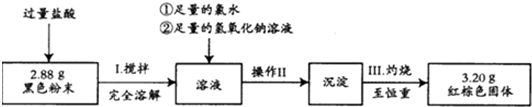
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定前对碱式滴定管仰视读数,滴定后又俯视,会使测定结果偏高 |
| B、滴定管和锥形瓶使用之前均需用所装溶液润洗 |
| C、用酚酞做指示剂,滴定终点是当最后一滴NaOH溶液滴入时,溶液颜色由无色变为浅红色,且半分钟内不变色 |
| D、滴定前锥形瓶内含有少量水对实验结果无影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com