
【题目】汽车内燃机燃烧时,在高温引发氮气和氧气反应会产生 NOx 气体,NOx 的消除是科研人员研究的重要课题。
(1)通过资料查得 N2(g)+O2(g)2NO(g)△H反应温度不平衡常数的关系如下表:
反应温度/℃ | 1538 | 2404 |
平衡常数 |
|
|
则△H___________________0(填“<”“>”戒“=”)
(2)在 800℃时,测得 2NO(g)+O2(g) 2NO2(g)的反应速率不反应物浓度的关系如下表所示
初始浓度/ | 初始速率/ | |
C0(NO) | C0(O2) | |
0.01 | 0.01 |
|
0.01 | 0.02 |
|
0.03 | 0.02 |
|
已知反应速率公式为 V 正=K 正×c m(NO)cn(O2),则 m=___________________, K 正=___________________L2mol-2s-1
(3)在某温度下(恒温),向体积可变的容器中充人 NO2 气体,发生反应 2NO2(g) N2O4(g),气体分压随时间的变化关系如图
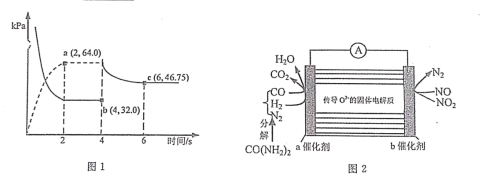
①该反应的压力平衡常数 KP=___________________。
②4s 时压缩活塞(活塞质量忽略不计)使容器体积变为原体积的 1/2,6s 时重新达到平衡,则P(N2O4)=___________________kPa。
(4)某学习小组利用图 2 装置探究向汽车尾气中喷入尿素溶液处理氮的氧化物。则该装置工作时,NO2 在 b 电极上的电极反应式为___________________。
【答案】> 2 2.5×10 3 ![]() 或 0.0625 136.6 2NO2+8e-4O2-+N2
或 0.0625 136.6 2NO2+8e-4O2-+N2
【解析】
(1)升高温度,K在变大,说明正向移动,升温向吸热反应方向移动即正向为吸热反应,则△H > 0。
(2)已知反应速率公式为 V 正=K 正×c m(NO)cn(O2),2.5×10-3 =K正×0.01m×0.01n,5×10-3 =K正×0.01m×0.02n,4.5×10-2 =K正×0.03m×0.02n,根据1、2两个等式相除得出n =1,根据2、3两个等式相除得出m=2,再根据第1个等式得出K正=2.5×103L2mol-2s-1。
(3)①该反应的压力平衡常数 KP=![]() 。
。
②4s时压缩活塞(活塞质量忽略不计)使容器体积变为原体积的1/2,6s时重新达到平衡,![]() 。
。
(4)根据图中信息得出NO2在b电极变为氮气,其电极反应式为2NO2+8e- = 4O2-+N2。
(1)升高温度,K在变大,说明正向移动,升温向吸热反应方向移动即正向为吸热反应,则△H > 0,故答案为:>。
(2)已知反应速率公式为 V 正=K 正×c m(NO)cn(O2),2.5×10-3 =K正×0.01m×0.01n,5×10-3 =K正×0.01m×0.02n,4.5×10-2 =K正×0.03m×0.02n,根据1、2两个等式相除得出n =1,根据2、3两个等式相除得出m=2,再根据第1个等式得出K正=2.5×103L2mol-2s-1,故答案为:2;2.5×103。
(3)①该反应的压力平衡常数 KP=![]() ,故答案为:
,故答案为:![]() 。
。
②4s时压缩活塞(活塞质量忽略不计)使容器体积变为原体积的1/2,6s时重新达到平衡,![]() ,则P(N2O4)=136.6 kPa。
,则P(N2O4)=136.6 kPa。
(4)根据图中信息得出NO2在b电极变为氮气,其电极反应式为2NO2+8e- = 4O2-+N2;故答案为:2NO2+8e- = 4O2-+N2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种高效的饮用水处理剂,工业上可由下列方法制得:Fe2O3+3Na2O2![]() 2Na2FeO4+Na2O,下列关于该反应的说法中正确的是( )
2Na2FeO4+Na2O,下列关于该反应的说法中正确的是( )
A.反应中Na2O2既是氧化剂又是还原剂
B.Fe2O3可以通过铁丝在氧气中燃烧制得
C.生成1molNa2FeO4,有3mol电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种有水果香味的油状液体,实验室通常用乙酸与乙醇在浓硫酸存在并加热的条件下反应生成乙酸乙酯。请回答:
(1)工业上常用乙烯水化法制备乙醇,乙烯的结构简式为____________。
(2)制备乙酸乙酯的化学方程式为__________________________,该反应的类型是_______反应。
(3)乙醇俗称酒精,是一种重要无污染的燃料和化工原料,乙醇的官能团为__________(写名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下反应均可生成![]() 。下列有关说法正确的是
。下列有关说法正确的是![]()
![]() 二氧化碳分解生成氧气:
二氧化碳分解生成氧气:![]() ;
;![]()
![]() 过氧化氢分解生成氧气:
过氧化氢分解生成氧气:![]() ;
;![]()
![]() 光照条件下,催化分解水蒸气生成氧气:
光照条件下,催化分解水蒸气生成氧气:![]() ;
;![]() 。
。
A.反应![]() 使用催化剂,能降低该反应的活化能
使用催化剂,能降低该反应的活化能
B.反应![]() 为吸热反应
为吸热反应
C.反应![]() 将化学能转化为光能
将化学能转化为光能
D.反应![]() ;
;![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把质量为mg的铜丝灼烧变黑,立即放入下列物质中,能使铜丝变红而且质量仍为mg的是
A.NaOH溶液B.CH3COOHC.稀HNO3D.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
下列说法错误的是( )
A.CH3OH转变成H2的反应不一定要吸收能量
B.1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ
C.反应①中的能量变化如图所示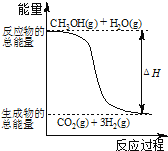
D.根据反应①和②推知:H2(g)+1/2O2(g)=H2O(g) ΔH=-241.9kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
(1)CH3CH2CH2COOH________,
(2)HCOOC2H5________,
(3)CH3CH2CH2CH2Cl________,
(4)CH3CHO________,
(5)![]() _________,
_________,
(6)![]() _________,
_________,
(7)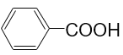 _________,
_________,
(8)CH3CH2CH=CHCH3_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应2A ( g)+B(g)![]() 2C(g),若经2 s后测得C的浓度为0.6 mol· L-1,现有下列几种说法,其中正确的是 ( )
2C(g),若经2 s后测得C的浓度为0.6 mol· L-1,现有下列几种说法,其中正确的是 ( )
A.用物质A表示的反应的平均速率为0.3 mol·L-1·s-1
B.用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
C.2 s时物质A的转化率为70%
D.2 s时物质B的浓度为0.7 mol · L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——有机化学基础]
某吸水材料与聚酯纤维都是重要化工原料,它们的合成路线如下:
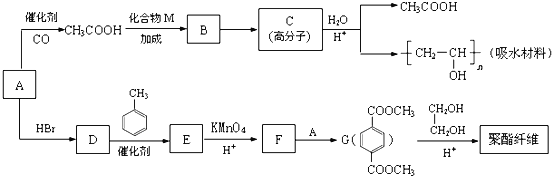
已知:①有机物A能与Na反应,相对分子质量为32。
②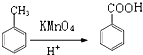
③RCOOR′+R″OH![]() RCOOR″+R′OH(R、R、R,代表烃基)
RCOOR″+R′OH(R、R、R,代表烃基)
(1)A的结构简式是____________,B中含氧官能团的名称是_____________。
(2)C的结构式是_______________,D→E的反应类型是_________________。
(3)F+A→G的化学方程式是_________________________。
(4)CH3COOH+CH≡CH→B的化学方程式是______________。
(5)G的同分异构体有多种,满足下列条件的共有___________种。
①苯环上只有两个取代基
②1mol与足量的NaHCO3溶液反应生成2mol CO2气体
(6)G→聚酯纤维的化学方程式是_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com