
(9分)(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有________离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是________(填字母)。
A.加入铜粉 B.加入铁粉 C.通入氯气 D.加入KSCN溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式 。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式 。
(3)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是________(填字母)。
A.铜粉 B.氯气 C.铁粉 D.KSCN溶液
(4)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是____nm,区别该液体和FeCl3溶液可用 方法。
(1) Fe2+ C 2Fe2++Cl2=2Fe3++2Cl- (2)2Fe3++Cu=2Fe2++Cu2+ (3)C (4) 1~100
丁达尔效应
【解析】
试题解析:(1)铁离子Fe3+,可以在溶液中加入硫氰酸钾溶液,溶液变为血红色,证明是含有三价铁离子;某溶液中加入KSCN溶液无明显现象,再滴加氯水,溶液立即变为血红色,说明原溶液含有亚铁离子,加入氯水发生反2Fe2++Cl2=2Fe3++2Cl-,生成的铁离子和硫氰酸根离子生成血红色溶液;要除去FeCl3溶液中少量的氯化亚铁,可行的办法是加入氧化剂,但不引入新的杂质,即通入氯气,对应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-;(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,对应的离子方程式为Cu+2Fe3+=2Fe2++Cu2+;(3)从使用过的腐蚀液中含铜离子,回收铜,可利用金属单质之间的置换反应,选项中只有铁粉能置换出Cu;(5)向沸水中逐滴滴加饱和FeCl3溶液,至液体呈透明的红褐色,生成氢氧化铁胶体,胶体的微粒直径的范围是1~100nm,区分胶体和FeCl3溶液可以通过丁达尔现象(效应),氢氧化铁胶体具有光亮的通路。
考点:铁及其化合物的性质


科目:高中化学 来源:2014-2015学年广东省汕头市高二上学期期中化学(文)试卷(解析版) 题型:?????
下列物质属于人体所需的糖类物质的是
A.淀粉 B.蛋白质 C.味精 D.食用油
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省武威市高一上学期期中化学试卷(解析版) 题型:选择题
标准状况下,ag气体A和bg气体B的分子数相同,下列说法不正确的是
A.气体A和B的相对分子质量之比为 a:b
B.同质量的气体A和B所含分子数目之比为b:a
C.标准状况下,气体A和B的密度之比为b:a
D.相同条件下,等体积的气体A和B的质量之比为a:b
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省武威市高二上学期期中化学(理)试卷(解析版) 题型:选择题
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g) N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确
A | B | C | D |
|
|
|
|
升高温度,平衡常数减小 | 0~3s内,反应速率为:v(NO2)=0.2mol?L-1 | t1时仅加入催化剂,平衡正向移动 | 到达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省武威市高二上学期期中化学(理)试卷(解析版) 题型:选择题
在一定温度下,下列叙述不是可逆反应A(气)+3B(气) 2C(气)+2D(固)达到平衡的标志的是
2C(气)+2D(固)达到平衡的标志的是
①C的生成速率与C的分解速率相等 ②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化 ④恒容下,混合气体的密度不再变化
⑤混合气体的总压强不再变化 ⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成 3amolB ⑧A、B、C、D的分子数之比为1:3:2:2
A.②⑧ B.②⑤⑧ C.①③④⑦ D.②⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期期中化学试卷(解析版) 题型:选择题
两份体积相同的某植物营养液,其配方如下:①②两份营养液的成分(所含离子)
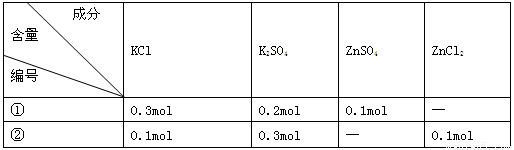
A.仅n(K+)相同 B.仅n(Cl-)相同 C.不完全相同 D.完全相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期期中化学试卷(解析版) 题型:选择题
下列各组离子中,能在无色溶液中大量共存的是
A、H+、Ca2+、Cl-、CO32- B、NO3-、Cl-、K+、H+
C、Na+、Fe3+、SO42-、OH- D、Na+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期第二次阶段测试化学试卷(解析版) 题型:选择题
下列溶液中,溶质的物质的量浓度为1mol/L的是
A、将40gNaOH溶于1L水所得的溶液
B、将80g SO3溶于水配成1L的溶液
C、将0.5mol/L的NaNO3溶液100mL加热蒸发掉50g水的溶液
D、含K+为2mol的K2SO4溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期月考化学理试卷(解析版) 题型:选择题
在容积可变的密闭容器中存在如下反应:2A(g)+2B(g) C(g)+3D(g) ΔH<0。
C(g)+3D(g) ΔH<0。
该可逆反应的反应速率-时间、转化率-时间关系图如下:

下列分析中不正确的是
A.图Ⅰ可体现t0时升高温度对反应速率的影响
B.图Ⅱ可体现t0时增大压强(缩小体积)或使用催化剂对反应速率的影响
C.图Ⅲ可体现催化剂对化学平衡的影响,且甲使用了催化剂
D.图Ⅲ可体现温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com