
【题目】在标准状况下,1体积水溶解700体积氨气,所得溶液密度为0.9gcm﹣3 , 这种氨水的物质的量浓度和溶质的质量分数分别为( )
A.18.4molL﹣134.7%
B.20.4molL﹣138.5%q2
C.18.4molL﹣138.5%
D.20.4molL﹣134.7%
【答案】A
【解析】解:NH3溶于水后虽然大部分生成NH3H2O,但在计算时,仍以NH3作为氨水中的溶质; 设水的体积为1L,氨气的体积为700L,
则氨气的物质的量为: ![]() =31.25mol,
=31.25mol,
氨气的质量为31.25mol×17g/mol=531.25g,
溶液的质量为1000g+31.25mol×17g/mol=1531.25g,
溶液的体积为= ![]() =1.7L,
=1.7L,
则氨水的质量分数为:w= ![]() ×100%=34.7%,
×100%=34.7%,
氨水的物质的量浓度为:c= ![]() =18.4 mol/L,
=18.4 mol/L,
故选A.
NH3溶于水后虽然大部分生成NH3H2O,但在计算时,仍以NH3作为氨水中的溶质,设水的体积为1L,则氨气的体积为700L,由标准状况下的体积可计算氨气的物质的量,溶液质量=氨气质量+水的质量,溶液体积可由溶液的质量和密度来计算,再根据质量分数定义、物质的量浓度的定义计算.


科目:高中化学 来源: 题型:
【题目】用![]() X表示原子:
X表示原子:
(1)中性原子的中子数:N=____。
(2)阳离子的中子数:AXn+共有x个电子,则N=____。
(3)阴离子的中子数:AXn-共有x个电子,则N=____。
(4)中性分子的中子数:12C16O2分子中,N=____。
(5)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为____ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成新燃料是发展低碳经济的重要方法,已知:CO(g) + 2H2(g)![]() CH3OH(g)是合成甲醇(CH3OH)的反应,该反应过程的能量变化如图所示,下列判断正确的是( )
CH3OH(g)是合成甲醇(CH3OH)的反应,该反应过程的能量变化如图所示,下列判断正确的是( )
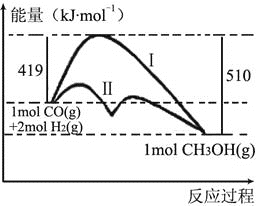
A. CO(g)与H2(g)反应生成1mol CH3OH(g)释放出91kJ的能量
B. 用碳制备原料气CO、H2的反应属于放热反应
C. 反应物总键能高于生成物的总键能
D. 若该反应生成液态CH3OH,则放出的能量更少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1: 
(1)海藻灼烧时是将带其放入(填仪器名称)中,用酒精灯充分加热灰化.
(2)指出提取碘的过程中有关的实验操作名称:①②、 .
(3)用CCl4从碘水中提取碘经过操作②后,有机溶剂在(填“上”或“下”)层,有机层呈色.
(4)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出图2实验装置中的错误之处并改正: 
①
② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为四种单质,常温时,A、B是气体,C、D是固体.E、F、G、H、I为五种化合物,F不溶水,E为气体且极易溶水成为无色溶液,G溶于水得黄棕色溶液.这九种物质间反应的转化关系如图所示 
(1)写出四种单质的化学式 ABCD
(2)写出H+B→G的离子方程式;
(3)写出G+I→H+D+E的化学方程式;
(4)某工厂用B制漂白粉. ①写出制漂白粉的化学方程式 .
②为测定该工厂制得的漂白粉中有效成分的含量,某该小组进行了如下实验:称取漂白粉3.0g,研磨后溶解,配置成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸(此时发生的离子方程式为:),静置.待完全反应后,用0.2molL﹣1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL.则该漂白粉中有效成分的质量分数为保留到小数点后两位).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z四种主族元素的单质在常温下都是气体,X、Y、Z对应的单质可以两两反应生成相应的A、B、C三个分子,其中B、C都是10电子且含有相同的元素X。A是一种难溶于水的有毒气体。他们之间还存在下列关系:
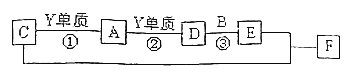
请回答下列问题:
(1)Z的原子结构示意图________,C的电子式为________。
(2)反应②的现象为______;写出反应③的化学方程式_________________________
(3)化合物F中含有的化合键为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A.原子的核外电子层数等于该元素所在的周期数
B.元素周期表中从IIIB族到IIB族10个纵行的元素都是金属元素
C.除氦外的稀有气体原子的最外层电子数都是8
D.同一元素的各种同位素的物理性质、化学性质均相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图。
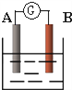
(1)若A为Pb,B为PbO2,电解质溶液为H2SO4溶液,电池的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。则该电池在工作时,A电极的质量将_______(填“增加”、“减小”或“不变”)。若该电池反应消耗了0.1mol H2SO4,则转移电子的数目为_______(设NA为阿伏加德罗常数的值)
(2)若A、B均为铂片,电解质溶液为KOH溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A极的电极反应式:__________________________;该电池工作一段时间后,溶液的碱性将___________(填“增强”、“减弱”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com