
| A、丙烯和环丙烷 |
| B、甲醛和乙酸 |
| C、乙酸和甲酸甲酯 |
| D、乙醛和乙酸乙酯 |


科目:高中化学 来源: 题型:
| A、氢氧化铍是两性氢氧化物 |
| B、B、Si的电负性数值相似 |
| C、Li和Mg的原子半径相近,且核外电子排布相近 |
| D、铍与盐酸或氢氧化钠溶液反应均能产生气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、质量数为35的氯原子:
| ||
B、BaSO4的电离方程式:BaSO4=Ba2++S
| ||
| C、乙烯的结构简式:C2H4 | ||
D、氯原子结构示意图: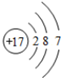 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28.58kJ |
| B、82.16 kJ |
| C、53.58 kJ |
| D、89.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑤⑥ | B、①④ |
| C、只有①④ | D、只有②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Fel2+Cl2=2FeCl3 |
| B、CaO+H2O=Ca(OH)2 |
| C、2H2O2=2H2O+O2 |
| D、Cl2+2NaBr=2NaCl+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 4 |
| 1 |
| 2 |
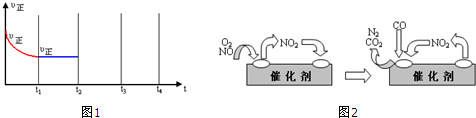
查看答案和解析>>
科目:高中化学 来源: 题型:
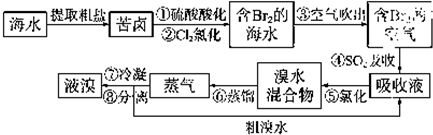
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com