
结合图判断,下列叙述正确的是( )
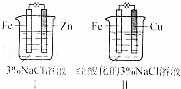
A.Ⅰ是验证牺牲阳极的阴极保护法的实验装置
B.Ⅰ和Ⅱ中负极反应均是Fe﹣2e﹣=Fe2+
C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e﹣=4OH﹣
D.Ⅰ和Ⅱ中分别加入少量K3Fe(CN)6溶液,均有蓝色沉淀
考点:原电池和电解池的工作原理.
专题:电化学专题.
分析:A、Ⅰ装置是原电池,锌做负极,铁做正极,发生的是锌的吸氧腐蚀;
B、Ⅰ中原电池负极为锌,Ⅱ为原电池,铁做负极;
C、Ⅰ装置是电解质溶液时中性溶液,属于吸氧腐蚀,Ⅱ装置中电解质溶液时酸性溶液,属于析氢腐蚀;
D、Ⅰ装置中不能生成亚铁离子,Ⅱ装置中负极铁失电子生成亚铁离子.
解答: 解:A、Ⅰ装置是原电池,锌做负极,铁做正极,发生的是锌的吸氧腐蚀,是验证牺牲阳极的阴极保护法的实验装置,故A正确;
B、Ⅰ中原电池负极为锌,电极反应为Zn﹣2e﹣=Zn2+,Ⅱ为原电池,铁做负极,电极反应为Fe﹣2e﹣=Fe2+,故B错误;
C、Ⅰ装置是电解质溶液时中性溶液,属于吸氧腐蚀,正极电极反应为:O2+2H2O+4e﹣=4OH﹣,Ⅱ装置中电解质溶液时酸性溶液,属于析氢腐蚀,正极电极反应为2H++2e﹣=H2↑,故C错误;
D、加入少量K3Fe(CN)6溶液,有蓝色沉淀是亚铁离子的性质,Ⅰ装置中不能生成亚铁离子,Ⅱ装置中负极铁失电子生成亚铁离子,故D错误;
故选A.
点评:本题考查了原电池原理的分析判断,注意电解质溶液不同,电极与电极反应变化,掌握基础是关键,题目难度中等.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
从A.甲醛 B.蛋白质 C.乙醇 D.聚苯乙烯 E.乙酸 F.淀粉六种有机物中选择合适的物质,将其标号填在空格内.
(1)羊毛的主要成分是灋.
(2)可用来检验碘单质的是灋.
(3)随意丢弃会造成“白色污染”的是.
(4)能用于除去热水瓶内胆中水垢〔主要成分:CaCO3,Mg(OH)2〕的是灋.
(5)某些装饰材料挥发出灋和苯等有毒物质会对空气造成污染.
(6)交警检测驾驶员呼出气体中的灋含量判断其是否酒驾.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热△H=﹣57.3kJ•mol﹣1,则H2SO4和Ba(OH)2反应的中和热△H=2×(﹣57.3)kJ•mol﹣1
B.CO(g)的燃烧热是283.0 kJ•mol﹣1,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0 kJ•mol﹣1
C.需要加热才能发生的反应一定是吸热反应
D.乙烷的燃烧热就是1mol乙烷燃烧生成气态水和二氧化碳所放出的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)⇌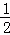 N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
电解原理在化学工业中有广泛应用.
(1)图1是电解食盐水的工业模拟图
①电解饱和食盐水的离子方程式
②溶液A是
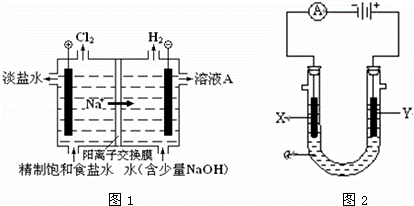
(2)图2是实验室常用的电解池装置,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①在X(填X或Y)极附近观察溶液变红.
②Y电极上的电极反应式为 ,检验该电极反应产物的方法是把
(3)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是 ,电极反应式是
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值.下列说法正确的是( )
A.0.56 L 甲烷中含有的共价键数为0.1NA
B.标准状况下,8g SO3含有的氧原子数为0.3NA
C.反应KClO3+6HCl═KCl+3Cl2↑+H2O中,每1 mol KClO3参与反应,转移e﹣数为6NA
D.pH=1的稀硫酸中含有的H+数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法不正确的是( )
A. 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B. 用过量氨水除去Fe3+溶液中的少量Al3+
C. 用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水
D. Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数,下列说法中正确的是
A.标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl-和ClO-两种粒子数之和为NA
B.80mL 10mol·L-1 盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA
C.含0.1 mol FeCl3的溶液完全水解后得到的胶体粒子个数为0.1 NA
D.含有4 NA个碳碳σ键的金刚石,其质量为24 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com