

 +nH2O.
+nH2O.分析 C在浓硫酸作用下生成D,D可发生加聚反应,可知C为HOCH2CH2COOH,D为CH2=CHCOOH,则E应含有两个酯基,至少含有4个O原子,如含4个O,则相对分子质量为$\frac{4×16}{48.5%}$=132,水解生成A、B,且A可转化为B,则A为醇,B为酸,E中无支链,结合相对分子质量可知E为HCOOCH2CH2COOCH3,则A为CH3OH,B为HCOOH,以此解答该题.
解答 解:C在浓硫酸作用下生成D,D可发生加聚反应,可知C为HOCH2CH2COOH,D为CH2=CHCOOH,则E应含有两个酯基,至少含有4个O原子,如含4个O,则相对分子质量为$\frac{4×16}{48.5%}$=132,水解生成A、B,且A可转化为B,则A为醇,B为酸,E中无支链,结合相对分子质量可知E为HCOOCH2CH2COOCH3,则A为CH3OH,B为HCOOH,
(1)C为HOCH2CH2COOH,含有羟基、羧基,D为CH2=CHCOOH,发生加聚反应,故答案为:羟基、羧基;加聚;
(2)由以上分析可知E的相对分子质量为132g/mol,结构简式为HCOOCH2CH2COOCH3,故答案为:132g/mol;HCOOCH2CH2COOCH3;
(3)反应②的化学方程式为CH3OH+O2$\stackrel{一定条件}{→}$HCOOH+H2O,反应③的化学方程式为nHOCH2CH2COOH$\stackrel{一定条件}{→}$ +n H2O,
+n H2O,
故答案为:CH3OH+O2$\stackrel{一定条件}{→}$HCOOH+H2O;nHOCH2CH2COOH$\stackrel{一定条件}{→}$ +n H2O;
+n H2O;
(4)C为HOCH2CH2COOH,能发生银镜反应的C的同分异构体应含有醛基,可为甲酸酯,对应的结构为HCOCH(OH)CH2OH;HCOOCH(OH)CH3;HCOOCH2CH2OH等,
故答案为:HCOCH(OH)CH2OH;HCOOCH(OH)CH3、HCOOCH2CH2OH.
点评 本题考查有机物推断,为高频考点,侧重于学生的分析能力的考查,题目涉及酯、醇、醛、羧酸、烯烃的性质与转化,关键是确定C为HOCH2CH2COOH,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体中的铁离子和氯离子可用渗析法除去 | |
| B. | 硬脂酸钠中混有少量的甘油,用盐析法除去 | |
| C. | 乙酸乙酯中混有少量乙酸,用饱和碳酸钠溶液洗涤后分液 | |
| D. | 氯化钠中有少量氯化铵,加过量的烧碱溶液后加热蒸干 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
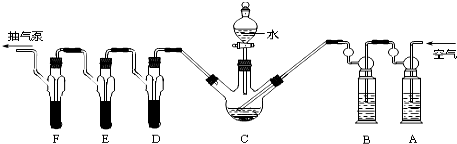
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去NaCl中少量的KNO3,可将固体混合物制成热饱和溶液,冷却结晶、过滤 | |
| B. | 探究“硫代硫酸钠与酸反应速率的影响因素”的实验中,通过观察产生浑浊的快慢,来反映试剂反应速率的大小.从而探究浓度,温度等外界条件对该反应的化学反应速率的影响 | |
| C. | 在中和热的测定实验中,应将碱液缓慢倒入酸液中,使反应充分进行 | |
| D. | 为了加快反应速率得到较干燥的硅酸白色胶状沉淀可以采用抽滤的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与氯气反应 | B. | CO通过灼热的三氧化二铁 | ||
| C. | 向氯化亚铁溶液中滴加双氧水 | D. | 铁与盐酸反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com