
【题目】下列叙述中,通常不能作为判断两种元素非金属性强弱的依据的是( )
A. 其气态氢化物的稳定性B. 单质的氧化性的强弱
C. 其最高价氧化物对应的水化物的酸性D. 单质的熔点高低
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①H2②铝 ③CaO ④CO2⑤H2SO4⑥Ba(OH)2⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为 .
(2)⑩在水中的电离方程式为 .
(3)少量的④通入⑥的溶液中反应的离子方程式为 , 过量的④通入⑥的溶液中反应的离子方程式为 .
(4)⑥与过量的碳酸氢钠溶液反应离子方程式: .
(5)②与⑨发生反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,当有5.4g Al发生反应时,转移电子的数目为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应N2+3H22NH3 , △H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图1所示: 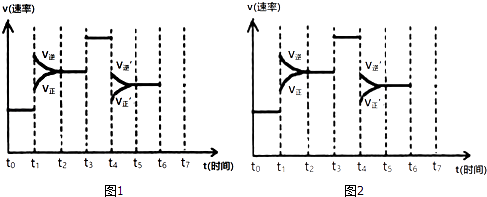
回答下列问题:
(1)处于平衡状态的时间段是(填选项).
A.t0~t1
B.t1~t2
C.t2~t3
D.t3~t4
E.t4~t5
F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是:t1时刻;t3时刻;t4时刻 . (填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中结论,下列时间段中,氨的百分含量最高的是(填选项).
A.t0~t1
B.t2~t3
C.t3~t4
D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,若将密闭容器体积缩小一半,则对反应产生的影响是(填选项).
A.正反应速率减小,逆反应速率增大
B.正反应速率增大,逆反应速率减小
C.正、逆反应速率都减小
D.正、逆反应速率都增大
(5)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图2中画出反应速率的变化曲线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( ) 
A.洗气瓶中产生的沉淀是碳酸钡
B.从Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是亚硫酸钡
D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
(1)写出电解饱和食盐水的离子方程式 .
(2)离子交换膜的作用为:、 .
(3)精制饱和食盐水从图中位置补充,氢氧化钠溶液从图中位置流出.(选填“a”、“b”、“c”或“d”)
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2 , 还生成CO2和KHSO4等物质.写出该反应的化学方程式 .
(5)室温下,0.1mol/LNaClO溶液的pH0.1mol/LNa2SO3溶液的pH.(选填“大于”、“小于”或“等于”)
(6)浓度均为0.1mol/L的N2SO3和Na2CO3的混合溶液中,SO32﹣、CO32﹣、HSO3﹣、HCO3﹣浓度从大到小的顺序为 .
(7)联氨(又称肼,N2H4 , 无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题: ①联氨分子的电子式为 .
②实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2Zn(OH)2ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2ZnCO3的工艺流程如图: 
请回答下列问题:
(1)当(NH4)2SO4 , NH3H2O的混合溶液中存在c(NH4+)=2c(SO42﹣)时,溶液呈(填“酸”、“碱”或“中”)性.
(2)“浸取”时为了提高锌的浸出率,可采取的措施是(任写一种).
(3)“浸取”时加入的NH3H2O过量,生成MnO2的离子方程式为 .
(4)适量S2﹣能将Cu2+等离子转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因: . [已知:Ksp(ZnS)=1.6×10﹣24 , Ksp(CuS)=1.3×10﹣36]
(5)“沉锌”的离子方程式为 .
(6)“过滤3”所得滤液可循环使用,其主要成分的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用芳香烃X和烯烃Y可以合成紫外线吸收剂BAD,BAD的结构简式为: 
已知G不能发生银镜反应.BAD的合成路线如下:
试回答下列问题
(1)写出结构简式:D .
(2)属于取代反应的有(填数字序号).
(3)1mol BAD最多可与含mol NaOH的溶液完全反应.
(4)写出下列反应的化学方程式:
反应④:
反应⑤: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下S2Cl2是橙黄色液体,其分子结构如图所示.少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液.下列关于S2Cl2的说法错误的是( ) 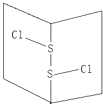
A.为非极性分子
B.分子中既含有极性键又含有非极性键
C.与S2Br2结构相似,熔沸点S2Br2>S2Cl2
D.与水反应的化学方程式可能为2S2Cl2+2H2O→SO2↑+3S↓+4HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com