
【题目】请用符号表示下列核素或同位素。
(1)质子数为![]() ,中子数为
,中子数为![]() 的
的![]() 原子:______。
原子:______。
(2)质子数和中子数都为9的氟原子:______。
(3)中子数为2的氢原子:______。
(4)中子数分别为8、9、10的氧原子:______。
(5)质量数分别为35、37的氯原子: ______。
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计以下实验。
Ⅰ.将![]() 溶液与
溶液与![]() 溶液混合生成
溶液混合生成![]() ,从而验证
,从而验证![]() 的碱性强于
的碱性强于![]() ,继而可以验证
,继而可以验证![]() 的金属性强于
的金属性强于![]() 。此设计 ______(填“合理”或“不合理”),理由是______。
。此设计 ______(填“合理”或“不合理”),理由是______。
Ⅱ.利用如图所示装置可以验证非金属性的变化规律。
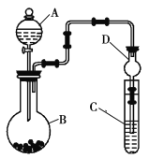
(1)仪器A的名称为______,干燥管D的作用是______。
(2)实验室中现有药品:![]() 溶液、
溶液、![]() 、浓盐酸、
、浓盐酸、![]() ,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为______、______、______,装置C中的实验现象为有黄色沉淀生成,相关反应的离子方程式为______。
,请选择合适的药品设计实验来验证氯的非金属性强于硫。装置A、B、C中所装药品分别为______、______、______,装置C中的实验现象为有黄色沉淀生成,相关反应的离子方程式为______。
(3)若要证明非金属性:![]() ,则A中加______,B中加
,则A中加______,B中加![]() ,C中加______,观察到C中的现象为______。
,C中加______,观察到C中的现象为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在AlCl3溶液中滴加过量的氨水,反应的化学方程式为__________________。
(2)碳酸氢钠与稀硫酸反应的离子方程式__________________;铜与浓硫酸共热反应的化学方程式__________________。
(3)现有0.284kg质量分数为10%的Na2SO4溶液,则溶液中Na2SO4的物质的量为______;配制250mL2.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液的体积_________mL。
(4)同一主族元素性质具有一定的相似性和递变性;同一主族,从上到下:原子的电子层数逐渐____________,原子半径逐渐____________;失电子能力逐渐____________,金属性逐渐____________ ;得电子能力逐渐 ___________,非金属性逐渐____________ 。
(5)A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,C是金属元素;A、C元素原子的最外层都只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;E元素原子最外层电子数比次外层电子数少1。回答下列问题:
写出E元素的元素符号:________画出B、C的原子结构示意图:B.________C________画出D的离子结构示意图:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
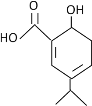
A.如图有机物核磁共振氢谱中出现8组峰
B.如图有机物分子式为C10H12O3
C.分子式为C9H12的芳香烃共有9种
D.蓝烷![]() 的一氯取代物共有6种(不考虑立体异构)
的一氯取代物共有6种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素形成的某种化合物(如图所示)是一种优良的防龋齿剂(用于制含氟牙膏)。下列说法错误的是( )
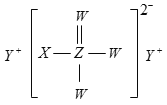
A.W、X、Y的简单离子的电子层结构相同
B.W、Y形成的化合物中只含离子键
C.该化合物中Z不满足8电子稳定结构
D.X、Y形成的化合物溶于水能促进水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解产物,某学生设计了如下实验方案:
淀粉液![]() 水解液
水解液![]() 混合液
混合液![]() 红色沉淀
红色沉淀
回答下列问题:
(1)试剂1是________,作用是___________________________。
(2)试剂2是________,作用是___________________________。
如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的________(填“能”或“不能”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.1996年人工合成了第112 号元素鎶(Cn),盛放鎶的容器上应该贴的标签是![]()
B.Na、Al、Cu可以分别用热还原法、热分解法和电解法冶炼得到
C.铜、冰醋酸、酒精分别属于强电解质、弱电解质、非电解质
D.煤的气化与液化均属于化学变化,煤的干馏属于物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M 的结构简式如下:下列有关M 叙述不正确的是( )
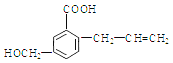
A. M的分子式为C11H12O3
B. 能使溴的四氯化碳溶液褪色
C. 一定条件下,M能生成高分子化合物
D. 能发生加成反应不能发生取代反应
【答案】D
【解析】
试题A.根据物质的结构简式可知M的分子式是C11H12O3,正确; B.该物质的分子中含有碳碳双键,因此能使溴的四氯化碳溶液褪色,正确;C. 该物质的分子中含有碳碳双键,在一定条件下发生加聚反应形成高聚物,正确;D. 化合物M含有碳碳双键,因此能发生加成反应,含有醇羟基、羧基,因此可以发生取代反应,错误。
考点:考查有机物的结构与性质的关系的知识。
【题型】单选题
【结束】
22
【题目】下列有关金属腐蚀与防护的说法不正确的是( )
A. 钢铁发生电化学腐蚀时,若表面水膜呈中性,则正极发生的反应为:2H2O+O2+4e一= 4OH一
B. 在潮湿的空气中,黄铜(铜锌合金)制品比纯铜制品更易产生铜绿
C. 金属制品在海水中比淡水中更容易发生腐蚀
D. 从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程
【答案】B
【解析】A、钢铁发生电化学腐蚀时,若表面水膜呈中性发生吸氧腐蚀,则正极发生的反应为:2H2O+O2+4e一=4OH一,A正确;B、在潮湿的空气中易发生电化学腐蚀,锌的金属性强于铜,因此黄铜(铜锌合金)制品比纯铜制品更不易产生铜绿,B错误;C、海水中含电解质浓度大,淡水中含电解质浓度小,故金属制品在海水中比淡水中更容易发生腐蚀,C正确;D、从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程,D正确;答案选B。
【题型】单选题
【结束】
23
【题目】下列说法不正确的是
A. 麦芽糖及其水解产物均能发生银镜反应
B. 用溴水即可鉴别苯酚溶液,2,4-已二烯和甲苯
C. 在酸性条件下,![]() 的水解产物是
的水解产物是![]() 和
和![]()
D. 用甘氨酸![]() 和丙氨酸
和丙氨酸![]() 缩合最多可形成4种二肽
缩合最多可形成4种二肽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是
A.用铁电极电解饱和食盐水:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B.Fe(NO3)3溶液中加入过量的HI溶液2Fe3++2I-=2Fe2++I2
C.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
D.向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com