
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 14g乙烯和丙烯的混合物中极性键数目为2NA
B. 标准状况下,![]() 与
与![]() 在光照条件下反应生成HCl分子数为
在光照条件下反应生成HCl分子数为![]()
C. 容器中2molNO与1molO2充分反应,产物的分子数为2NA
D. 电解精炼铜时阳极减轻32 g,电路中转移电子数目一定为NA
【答案】A
【解析】
A.乙烯和丙烯最简式是CH2,最简式的式量是14,所以14g乙烯和丙烯的混合物中含有1molCH2,则其中含有的极性键C-H数目为2NA,A正确;
B.取代反应是逐步进行的,不可能完全反应,所以标准状况下,22.4LCH4与Cl2在光照条件下反应生成HCl分子数小于4NA,B错误;
C.容器中2molNO与1molO2充分反应会产生2molNO2,NO2会有部分发生反应产生N2O4,因此最后得到的气体分子数目小于2NA,C错误;
D.在阳极反应的金属有Cu,还有活动性比Cu强的金属,因此电解精炼铜时阳极减轻32 g,电路中转移电子数目不一定为NA,D错误;
故合理选项是A。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】滴定分析法又叫容量分析法,是一种重要的定量分析法。酸碱中和滴定是重要的滴定分析实验。
(1)现用已知浓度的NaOH溶液,用中和滴定法去测定未知浓度的CH3COOH溶液,实验步骤如下,请填写有关内容:
① 将酸式滴定管洗净后,每次用3~4 mL待测醋酸溶液润洗2~3次,然后加入待测醋酸至0刻度以上。把滴定管夹在滴定管夹上,转动活塞,放出少量溶液,使滴定管________,并使液面达到________,记录初始读数。
② 用相似的方法在碱式滴定管中加入标准NaOH溶液,并调节好液面。
③ 在酸式滴定管内取V mL的待测醋酸移到洗净的锥形瓶中,加2~3滴________作指示剂。
④ 用标准NaOH溶液滴定待测醋酸。左手________,向锥形瓶中慢慢滴加NaOH溶液,右手轻轻摇动锥形瓶,两眼注视________,当溶液颜色由无色变为粉红色,且半分钟内不褪色,表示达到滴定终点,记录终点读数。
⑤ 重复上述实验步骤。
(2) 指示剂的选择一般根据滴定突跃,其选择标准是________。
(3) 已知标准NaOH溶液的浓度为0.1000 mol·L-1,所取待测醋酸的体积V均为20.00 mL。实验过程记录的数据如下表,求待测醋酸的物质的量浓度________。
滴定前 | 第一次 终点 | 第二次 终点 | 第三次 终点 | |
碱式滴定管 液面刻度 | 0.10 mL | 19.12 mL | 18.15 mL | 19.08 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。废旧电池正极片(磷酸亚铁锂、炭黑和铝箔等)可再生利用,其工艺流程如下:

已知:碳酸锂在水中的溶解度,0℃时为1.54g,90℃时为0.85g,100℃时为0.71g。
(1)上述流程中至少需要经过______次过滤操作。
(2)“氧化”发生反应的离子方程式为__________;若用HNO3代替H2O2不足之处是_____。
(3)①已知Ksp[Fe(OH)3]=2.6×10-39。常温下,在Fe(OH)3悬浊液中,当溶液的pH=3.0时,Fe3+的浓度为________mol/L。
②实际生产过程中,“调节pH”生成沉淀时,溶液pH与金属元素的沉淀百分率(ω)的关系如下表:
pH | 3.5 | 5.0 | 6.5 | 8.0 | 10.0 | 12.0 |
ω(Fe)/% | 66.5 | 79.2 | 88.5 | 97.2 | 97.4 | 98.1 |
ω(Li)/% | 0.9 | 1.3 | 1.9 | 2.4 | 4.5 | 8.0 |
则最佳的沉淀pH=________。
(4)“沉锂" 时的温度应选(填标号)______为宜,并用___洗涤(填“热水" 或“冷水")。
a.90℃ b.60 ℃ c.30 ℃ d.0 ℃
(5)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池放电时正极的电极反应式为________。
(6)工业上可以用FePO4、Li2CO3和H2C2O4作原料高温焙烧制备 LiFePO4,该反应的化学方程式为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨甲环酸(F)又称止血环酸、凝血酸,是一种在外科手术中广泛使用的止血药,可有效减少术后输血。氨甲环酸(F)的一种合成路线如下(部分反应条件和试剂未标明):

(1)B的系统命名为_______;反应①的反应类型为_____。
(2)化合物C含有的官能团的名称为_____。
(3)下列有关氨甲环酸的说法中,正确的是_____(填标号)。
a.氨甲环酸的分子式为C8H13NO2
b.氨甲环酸是一种天然氨基酸
c.氨甲环酸分子的环上一氯代物有4种
d.由E生成氨甲环酸的反应为还原反应
(4)氨甲环酸在一定条件下反应生成高分子化合物的化学方程式为________。
(5)写出满足以下条件的D的同分异构体的结构简式_____。
①属于芳香族化合物 ②具有硝基 ③核磁共振氢谱有3组峰
(6)写出用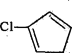 和CH2=CHOOCCH3为原料制备化合物
和CH2=CHOOCCH3为原料制备化合物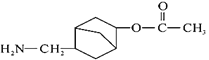 的合成路线(其他试剂任选)。_____
的合成路线(其他试剂任选)。_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是指导化学学习的重要工具,下图为元素周期表的一部分,请按要求填空:

(1)N在元素周期表中的位置是______________ ;N和F处于同一行,是由于它们的 __________ 相同。
(2)以上元素中,原子半径最小的是 ________ (写元素符号);最高价氧化物对应水化物中酸性最强的是 ______________ (写化学式)。
(3)Mg和Al中,金属性较强的是 __________ (写元素符号),写出一条能说明该结论的事实_________________________________。
(4) S和Cl中,非金属性较强的是 __________ (写元素符号),不能说明该结论的事实是_________。
a.氯气与铁反应生成 FeCl3,硫与铁反应生成FeS
b.把 Cl2通入 H2S溶液中能发生置换反应
c.受热时 H2S易分解,HCl不易分解
d.单质硫是固体,氯的单质是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】降冰片二烯类化合物是一类太阳能储能材料。降冰片二烯在紫外线照射下可以发生下列转化。下列说法错误的是( )
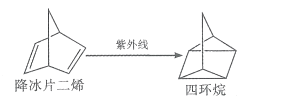
A. 降冰片二烯与四环烷互为同分异构体
B. 降冰片二烯能使酸性高锰酸钾溶液褪色
C. 四环烷的一氯代物超过三种(不考虑立体异构)
D. 降冰片二烯分子中位于同一平面的碳原子不超过4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H(3一溴-5-甲氧基苯甲酸甲酯)是重要的有机物中间体,可以由A(C7H8)通过下图路线 合成。

请回答下列问题:
(1)C的化学名称为________,G中所含的官能团有醚键、_______、__________(填名称)。
(2)B的结构简式为________,B生成C的反应类型为___________。
(3)由G生成H的化学方程式为_________。E→F是用“H2/Pd”将硝基转化为氨基,而C→D选用的是(NH4)2S,其可能的原因是________。
(4)化合物F的同分异构体中能同时满足下列条件的共有________种。
①氨基和羟基直接连在苯环上 ②苯环上有三个取代基且能发生水解反应
(5)设计用对硝基乙苯 为起始原料制备化合物
为起始原料制备化合物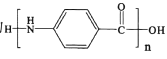 的合成路线(其他试剂任选)。_____
的合成路线(其他试剂任选)。_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物Z可用于防治骨质疏松,可通过X、Y经两步转化得到Z。下列说法正确的是( )
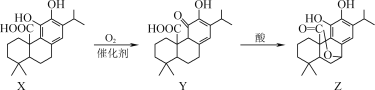
A. X、Y、Z都属于芳香族化合物
B. Y分子中含有3个手性碳原子
C. X、Y、Z与浓溴水反应最多消耗1molBr2
D. 1molZ与NaOH溶液反应最多消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知A、B、C、D四种分子所含原子的数目依次为1、3、6、6,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1∶2。D是一种有毒的有机物。
(1)组成A分子的原子的元素符号是________。
(2)从B分子的立体结构判断,该分子属于________分子(填“极性”或“非极性”)。
(3)C分子中都包含________个σ键,________个π键。
(4)D的熔、沸点比C2H6的熔、沸点高,其主要原因是(需指明D是何物质):________。
Ⅱ.CO的结构可表示为CO,N2的结构可表示为NN。
(5)下表是两者的键能数据:(单位:kJ·mol-1)

结合数据说明CO比N2活泼的原因: ____________________。
Ⅲ.Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关。
(6)基态Ni原子的核外电子排布式为________,基态Cu原子的价电子排布式为________。
(7)Fe(CO)5常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于________(填晶体类型)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com