
请在标有序号的空白处填空。
(1)可正确表示原子轨道的是____①____。
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)原子的电子排布式:____②____。
(3)下列物质变化,只与范德华力有关的是__③____。
A.干冰熔化
B.乙酸汽化
C.乙醇与丙酮混溶
D.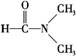 溶于水
溶于水
E.碘溶于四氯化碳
F.石英熔融
(4)下列物质中,只含有极性键的分子是____④____,既含离子键又含共价键的化合物是____⑤____;只存在σ键的分子是____⑥____,同时存在σ键和π键的分子是____⑦____。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6
F.CaCl2 G.NH4Cl
(5)用“>”“ <”或“=”填空:
第一电离能的大小:Mg____⑧____Al;
熔点的高低:KCl____⑨____MgO。
【解析】(1)主量子数为2的能级包括s、p;主量子数为3的能级包括s、p、d;
(2)镓(Ga)的原子序数为31,电子分布的能级为1s、2s、2p、3s、3p、3d、4s、4p。
(3)范德华力存在于分子之间,不含氢键的分子晶体符合题目要求。乙酸、乙醇 、
、 分子间存在氢键,石英为原子晶体,熔融时破坏的是共价键。
分子间存在氢键,石英为原子晶体,熔融时破坏的是共价键。
(4)不同 元素的原子之间形成的共价键为极性键,同种原子之间形成的共价键是非极性键;活
元素的原子之间形成的共价键为极性键,同种原子之间形成的共价键是非极性键;活 泼金属元素和活泼非金属元素形成离子键,铵盐中存在离子键;只形成单键的共价键只存在σ键,含有双键或三键的物质同时存在σ键和π键。故只含有极性键的是CH2Cl2、CO2;既含有离子键又含有共价键
泼金属元素和活泼非金属元素形成离子键,铵盐中存在离子键;只形成单键的共价键只存在σ键,含有双键或三键的物质同时存在σ键和π键。故只含有极性键的是CH2Cl2、CO2;既含有离子键又含有共价键 的化合物是NH4Cl;只存在σ键的分子是CH2Cl2、C2H6;同时存在σ键和π键的分子是N2、CO2、C2H4。
的化合物是NH4Cl;只存在σ键的分子是CH2Cl2、C2H6;同时存在σ键和π键的分子是N2、CO2、C2H4。
(5)同周期从左到右第一电离能增大,但第2、3、4周期中第ⅡA族的第一电离能比相邻的第ⅠA和第ⅢA族的大;KCl与MgO均为离子晶体,晶格能的大小决定熔点高低,KCl与MgO晶胞类型相同,半径r(K+)>r(Mg2+),电荷Mg2+>K+,故MgO的晶格能大于KCl,故熔点KCl<MgO。
答案:①A、C ②1s22s22p63s23p63d104s24p1
③ A、E ④B、C ⑤G ⑥C、E ⑦A、B、D
A、E ④B、C ⑤G ⑥C、E ⑦A、B、D
⑧> ⑨<


科目:高中化学 来源: 题型:
下列描述正确的是
A.氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同
B.滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存
C.某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42-
D.Fe(NO3)2溶液中滴加少量稀硫酸会变黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
无机化合物A中含有元素Li元素,A的摩尔质量23g·mol-1,A主要用于有机合成和药物制造,同时也是良好的储氢材料。在一定条件下,0.1mol固体A与0.1molNH4Cl固体恰好完全反应,生成固体B和4.48L(标准状况)气体C。已知气体C极易溶于水,且得到碱性溶液。电解无水B可生成金属单质D和氯气。请回答下列问题:
(1)A的化学方式是_________________________。
(2)写出化合物A与NH4Cl反应的化学方程式:_______________________________。
(3)某同学通过查阅资料得知物质A的性质:
I.工业上可用金属D与液态的C在硝酸铁催化下反应来制备A物质。
II.物质A遇水强烈水解,释放出气体C。
①I中发生反应的基本反应类型是__________________________。
②物质A遇水强烈水解的化学方程式为_________________________。
(4)工业制备单质D的流程如下:
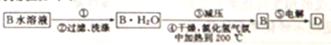
①步骤①中操作的名称为________________。
②试用平衡原理解释步骤③中减压的目的是:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属的说法中,正确的是
①纯铁不容易生锈 ②钠着火用水扑灭 ③KSCN溶液可以检验Fe3+
④缺钙会引起骨质疏松,缺铁会引起贫血 ⑤青铜、不锈钢、硬铝都是合金
A.①③④ B.②③④⑤ C.①③④⑤ D.①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )。
A.用加热法可除去Na2CO3中的NaHCO3
B.Na2CO3的热稳定性大于NaHCO3
C.可用石灰水区分Na2CO3与NaHCO3溶液
D.小苏打可中和胃酸、热纯碱可除去油污
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的四种元素A、B、C、D分别处于第1~4周期,其中A原子核是一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D原子外围电子排布为3d104s1。请回答下列问题:
(1)这四种元素中电负性最大的是______(填元素符号,下同),第一电离能最小的是________;
 (2)C所在的主族元素气态氢化物中,沸点最低的是______(填化学式);
(2)C所在的主族元素气态氢化物中,沸点最低的是______(填化学式);
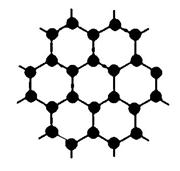
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如右图所示,其原子的杂化类型为____________;
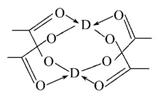 (4)D的醋酸盐晶体局部结构如右图,该晶体中含有的化学键是______(填选项序号);
(4)D的醋酸盐晶体局部结构如右图,该晶体中含有的化学键是______(填选项序号);
①极性键 ②非极性键
③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如下图:
D单质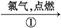 棕色的烟
棕色的烟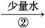 绿色溶液
绿色溶液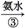 蓝色沉淀
蓝色沉淀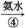 蓝色溶液
蓝色溶液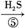 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,[SO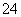 ]>[NH
]>[NH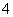 ]
]
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1 mol·L-1的氨水中加入少量硫酸铵固体,则溶液中 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事故处理措施正确的是 ( )
A.金属钠着火,立即用泡沫灭火器灭火
B.在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷的纯度
C.酒精灯不慎着火,应立即吹熄
D.眼睛里溅进盐酸,立即用NaOH溶液洗涤眼睛
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com