
盐泥是氯碱工业中的废渣,主要成分是镁的硅酸盐和碳酸盐(含少量铁、铝、钙的盐)。实验室以盐泥为原料制取MgSO4·7H2O的实验过程如下:
―→―→产品
已知:①室温下Ksp[Mg(OH)2]=6.0×10-12。②在溶液中,Fe2+、Fe3+、Al3+从开始沉淀到沉淀完全的pH范围依次为7.1~9.6、2.0~3.7、3.1~4.7。③三种化合物的溶解度(S)随温度变化的曲线如图所示。

(1)在盐泥中加入稀硫酸调pH为1~2以及煮沸的目的是_____________________。
(2)若室温下的溶液中Mg2+的浓度为6.0 mol·L-1,则溶液pH≥________才可能产生Mg(OH)2沉淀。
(3)由滤液Ⅰ到滤液Ⅱ需先加入NaClO调溶液pH约为5,再趁热过滤,则趁热过滤的目的是__________________,滤渣的主要成分是______________________。
(4)从滤液Ⅱ中获得MgSO4·7H2O晶体的实验步骤依次为①向滤液Ⅱ中加入______________;②过滤,得沉淀;③________________;④蒸发浓缩,降温结晶;⑤过滤、洗涤得产品。
(5)若获得的MgSO4·7H2O的质量为24.6 g,则该盐泥中镁[以Mg(OH)2计]的百分含量约为________(MgSO4·7H2O的相对分子质量为246)。
(1)提高Mg2+的浸取率(其他合理答案均可)
(2)8
(3)温度较高时钙盐与镁盐分离得更彻底(或高温下CaSO4·2H2O溶解度小等合理答案均可) Al(OH)3、Fe(OH)3、CaSO4·2H2O
(4)NaOH溶液 向沉淀中加足量稀硫酸(合理答案均可)
(5)20.0%
【解析】(1)加入H2SO4可以使Mg的硅酸盐或碳酸盐充分转化成Mg2+。(2)c(OH-)=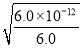 mol·L-1=10-6 mol·L-1,所以pH=8。(3)加入NaClO,可以把Fe2+氧化成Fe3+,当pH大约为5时,Fe3+、Al3+转化成沉淀;根据溶解度曲线,温度高时,CaSO4·2H2O的溶解度更小,所以滤渣的主要成分为Al(OH)3、Fe(OH)3和CaSO4·2H2O。(4)使Mg2+转化成MgSO4·7H2O的步骤为①加入NaOH溶液。②过滤得Mg(OH)2沉淀。③加入稀H2SO4。④蒸发浓缩、降温结晶、过滤得产品。(5)根据镁元素守恒得
mol·L-1=10-6 mol·L-1,所以pH=8。(3)加入NaClO,可以把Fe2+氧化成Fe3+,当pH大约为5时,Fe3+、Al3+转化成沉淀;根据溶解度曲线,温度高时,CaSO4·2H2O的溶解度更小,所以滤渣的主要成分为Al(OH)3、Fe(OH)3和CaSO4·2H2O。(4)使Mg2+转化成MgSO4·7H2O的步骤为①加入NaOH溶液。②过滤得Mg(OH)2沉淀。③加入稀H2SO4。④蒸发浓缩、降温结晶、过滤得产品。(5)根据镁元素守恒得 ×100%=20%。
×100%=20%。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014高考化学二轮专题突破 专题十一常见金属元素练习卷(解析版) 题型:选择题
下列各组物质中,物质之间通过一步反应就能实现图示变化的是( )
物质编号 | 物质转化关系 | a | b | c | d |
① |
| FeCl2 | FeCl3 | Fe | CuCl2 |
② | NO | NO2 | N2 | HNO3 | |
③ | Na2O | Na2O2 | Na | NaOH | |
④ | Al2O3 | NaAlO2 | Al | Al(OH)3 |
A.①④ B.①②③ C.①③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题五离子反应练习卷(解析版) 题型:选择题
下列有关的离子方程式正确的是( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4+
B.铜片接电源正极,碳棒接电源负极,电解硫酸溶液:Cu+2H+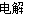 Cu2++H2↑
Cu2++H2↑
C.磷酸一氢钠溶液水【解析】
HPO42-+H2O PO43-+H3O+
PO43-+H3O+
D.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH-
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题二化学用语及常用计量练习卷(解析版) 题型:选择题
下列化学用语的使用正确的是( )
A.K+与Ar的结构示意图相同
B.Na2O的电子式是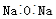
C.通常状况下,1.5 mol氧气与0.5 mol氮气混合后气体的总体积为44.8 L
D.乙烷、乙烯和苯的结构简式分别为CH3CH3、CH2=CH2和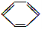
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题九化学反应速率化学平衡练习卷(解析版) 题型:选择题
一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:
2SO2(g)+O2(g)  2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | t1 | t2 | t3 | t4 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
A.反应在前t1s的平均速率v(O2)=0.4/t1 mol·L-1·s-1
B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C.相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题三溶液组成的计量及其应用练习卷(解析版) 题型:选择题
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是( )
①w=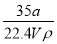 ×100%
×100%
②c=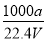
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w
④若上述溶液中再加入0.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为c(NH4+)>c(Cl-)>c(OH-)>c(H+)
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题三溶液组成的计量及其应用练习卷(解析版) 题型:选择题
下图是某同学用500 mL容量瓶配制0.10 mol·L-1 NaOH溶液的过程:
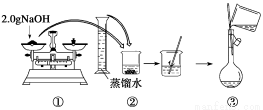
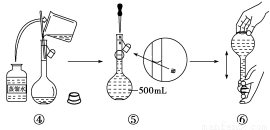
该同学的错误步骤有( )
A.1处 B.2处 C.3处 D.4处
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮专题突破 专题一物质的组成性质和分类练习卷(解析版) 题型:填空题
(1)现有以下物质:
aNaCl晶体;b液态SO3;c液态的醋酸;d汞;eBaSO4固体;f纯蔗糖;g酒精;h熔化的KNO3
请回答下列问题(填写相应的字母):
①以上物质中能导电的是________。
②以上物质中属于电解质的是____________。
③以上物质中属于非电解质的是____________。
④以上共价化合物中溶于水后形成的水溶液能导电的是______________。
(2)下列关于氧化物的各项叙述正确的是__________(填写序号)。
①酸性氧化物肯定是非金属氧化物 ②非金属氧化物肯定是酸性氧化物 ③碱性氧化物肯定是金属氧化物 ④金属氧化物都是碱性氧化物 ⑤酸性氧化物均可与水反应生成相应的酸 ⑥与水反应生成酸的氧化物不一定是酸酐,与水反应生成碱的氧化物不一定是碱性氧化物 ⑦不能跟酸反应的氧化物一定能跟碱反应
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题7电解质溶液练习卷(解析版) 题型:选择题
现有0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大;②c(NH3·H2O)增大;③N 数目增多;④c(OH-)增大;⑤导电性增强;⑥
数目增多;④c(OH-)增大;⑤导电性增强;⑥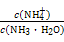 增大
增大
A.①②③ B.①③⑤ C.①③⑥ D.②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com