
A、Al3+、Ag+、NO
| ||||
B、Cu2+、NH
| ||||
| C、Ba2+、K+、Cl-、Br- | ||||
D、Zn2+、Na+、NO
|
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾可用作净水剂 |
| B、干冰能用于制冷剂 |
| C、过氧化钠可以漂白任何有色物质 |
| D、小苏打是一种膨松剂,可用于制作馒头和面包 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.74 | 0.75 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
| A、X与Y可以形成阴离子XY32- |
| B、元素R的含氧酸一定为强酸 |
| C、Z的氢化物的沸点比T的氢化物的沸点高 |
| D、由X形成的化合物QX和XR4,其晶体类型不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
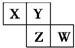 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )| A、元素Y和元素Z的氢化物中均只存在极性共价键 |
| B、单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C、元素W的最高价氧化物对应水化物的酸性最强 |
| D、元素Y和元素Z的最高正化合价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、Na+、SO42-、H2O2 |
| B、C2H5OH、MnO4-、H+、K+ |
| C、Pb2+、K+、SO42-、Cl- |
| D、Na+、SO32-、CH3COO-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠的化学性质很活泼,钠离子和钠原子都具有较强的还原性 |
| B、钠能把钛锆等金属从它们的盐溶液中还原出来 |
| C、钠与氧气反应的产物与反应条件有关 |
| D、钠和钾的合金在室温下呈固态,可作原子反应堆的导热剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol CO2 的体积为22.4L |
| B、CO2的摩尔质量为44g |
| C、64g SO2含有氧原子数2NA |
| D、NA个CO2的质量(g)与CO2的相对分子质量数值相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com