
| 5.6��10-3L |
| 22.4L/mol |
| ||
| ||
| 5.6��10-3L |
| 22.4L/mol |
| 0.01mol |
| 0.025L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������һ�������Դ����������ȡ������������Դ������о��ȵ�
������һ�������Դ����������ȡ������������Դ������о��ȵ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ���ش����⣺
��ͼ���ش����⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| KMnO4/H+ |
 ��-R1��-R2��ʾ��ԭ�ӻ���������
��-R1��-R2��ʾ��ԭ�ӻ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
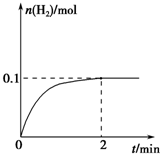 ��-��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
��-��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��a������d���� |
| B��c�缫������ԭ��Ӧ |
| C���������У�d�缫�������� |
| D���������У�������Ũ�Ȳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��[SiO4]��������ṹ�� |
| B��C2H5Cl��NaOH��Һ��ϼ���ˮ�����AgNO3��Һ���Լ���Cl- |
| C����MgCl2�����к��й��ۼ������Ӽ� |
| D��0.5g C3H4�к��й��õ��ӶԵ���ĿΪ1��6.02��1023 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com