
| A、阴极只析出H2 |
| B、阳极先析出Cl2,后析出O2 |
| C、电解最后阶段为电解水 |
| D、溶液pH不断增大,最后为7 |
| ||
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜作阳极,锌作阴极,硫酸铜作电解质溶液 |
| B、锌作阳极,铜作阴极,硫酸锌作电解质溶液 |
| C、铁接在直流电源的正极,银接在直流电源的负极,硝酸银溶液作电解质溶液 |
| D、铁接在直流电源的负极,银接在支流电源的正极,硝酸银溶液作电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
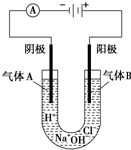 如图所示表示的是电解饱和食盐水的装置,阴极材料是铁棒,阳极材料是碳棒,饱和食盐水中含有少量酚酞.
如图所示表示的是电解饱和食盐水的装置,阴极材料是铁棒,阳极材料是碳棒,饱和食盐水中含有少量酚酞.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5mol/L |
| B、1mol/L |
| C、0.8mol/L |
| D、1.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
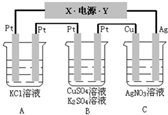 如图所示,若电解5min时铜电极质量增加2.16g,试回答:
如图所示,若电解5min时铜电极质量增加2.16g,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com