本题为选做题,包括A、B两题.选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题.若两题都作答,则以A题计分.
A.《化学与生活》
(1)食品和药品关系人的生存和健康.
①市场上销售的食盐品种很多.下列食盐中,所添加的元素不属于人体必需微量元素的是
(填字母).
A.加锌盐 B.加碘盐 C.加钙盐
②纤维素被称为“第七营养素”.食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质.从化学成分看,纤维素是一种
(填字母).
A.多糖 B.蛋白质 C.脂肪
③某同学感冒发烧,他可服用下列哪种药品进行治疗
(填字母).
A.麻黄碱 B.阿司匹林 C.抗酸药
(2)材料是人类赖以生存和发展的重要物质基础.
①生产硅酸盐水泥和普通玻璃都需用到的共同的主要原料是
.
②生活中有大量的铝制品.家用铝锅不能经常用热碱水洗涤去污,原因是(用离子方程式表示)
.
③有机玻璃受热时会软化,易于加工成型.有机玻璃是一种
材料(选填“硅酸盐”或“纤维”或“塑料”).导电塑料的结构可表示为

,则其单体的结构简式为
.
(3)保护环境、保护地球是人类共同的呼声.
①向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO
2.发生反应的化学方程式为
.
②天然水中含有的细小悬浮颗粒可以用
做混凝剂(写名称)进行净化处理.工业废水中含有的Cr
3+离子,可用熟石灰作沉淀剂,在pH为8~9时生成沉淀而除去,该反应的离子方程式是
.
③城市餐饮业会产生大量污染环境的“地沟油”.“地沟油”的主要成分是油脂.综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和
.生活中会产生大量废弃塑料,将废弃塑料进行
处理,可以获得乙烯、丙烯等化工原料.
B.《有机化学基础》
(1)有机物含有的官能团不同,性质也有差异.
①1mol下列有机物可与2mol溴单质发生加成反应的是
(填字母).
A.乙烯 B.乙炔 C.乙烷
②下列有机物中,核磁共振氢谱只有一个吸收峰的是
(填字母).
A.苯 B.苯酚 C.苯甲酸
③下列有机物中,能发生银镜反应的是
(填字母).
A.乙酸乙酯 B.乙醇 C.葡萄糖
(2)分子式为C
4H
10O,属于醇的同分异构体有
种,其中一种不能氧化成醛或酮,它的结构简式是
;另一种没有支链且能被氧化成醛,写出它与乙酸发生酯化反应的方程式
.
(3)科学家常采用将药物连接在高分子载体上,制成缓释长效药物.已知某种解热镇痛类药物,其结构简式为A,把它连接到高分子聚合物B上,形成缓释长效药物C.
A

C

①高分子聚合物B的结构简式为
.
②A与B反应生成C的反应类型是
.
③A可水解成
和
(写结构简式).



 ,则其单体的结构简式为
,则其单体的结构简式为


 Ⅰ、碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g).
Ⅰ、碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)?WI2(g).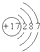 所表示的原子是
所表示的原子是