



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ũ���� | B������ |
| C��˫��ˮ | D��Ư�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��11.2L NO��11.2L O2��Ϻ�ķ�������ΪNA |
| B��1mol����ϩ�к��е�̼̼˫����Ϊ4NA |
| C��50mL 18.4mol/LŨ����������ͭ�ȷ�Ӧ������SO2������ĿΪ0.46NA |
| D��1mol Fe��������ϡHNO3��Ӧ���ų�NO��N2O��ת��3NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��BaSO4��BaCO3�ܽ��С�����ԣ�BaCO3������ת��ΪBaSO4 | ||
| B��BaCO3��BaSO4��������ˮ�����Զ������������Լ� | ||
C���κ��¶��£���Na2CO3��Һ�м���BaCl2��Na2SO4�������ֳ�������ʱ��
| ||
| D�����¶��£�BaCO3��Ҫ��Na2SO4��Һ��ת��ΪBaSO4����Na2SO4Ũ������Ϊ2.2��10-6mol?L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
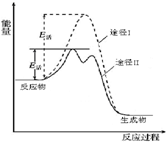 ���ĵ��ʺͻ������ڹ�ũҵ���������Ź㷺��Ӧ�ã�
���ĵ��ʺͻ������ڹ�ũҵ���������Ź㷺��Ӧ�ã�
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
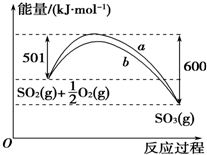 2013���ҹ�ú̿����35.2�ڶ֣�Լռһ����Դ��������78.6%��ú̿��������35.7�ڶ֣�Լռһ����Դ��������72.8%���й���úȱ����������Դ��Դ״���������ڽ��ϳ�ʱ���ڣ�ú̿�Խ����й�����Ҫ��Դ��
2013���ҹ�ú̿����35.2�ڶ֣�Լռһ����Դ��������78.6%��ú̿��������35.7�ڶ֣�Լռһ����Դ��������72.8%���й���úȱ����������Դ��Դ״���������ڽ��ϳ�ʱ���ڣ�ú̿�Խ����й�����Ҫ��Դ��| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
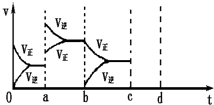 ��1����ͼ��ʾ���ܱ������з�Ӧ��2SO2+O2?2SO3��H��0�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����ab�����иı������������
��1����ͼ��ʾ���ܱ������з�Ӧ��2SO2+O2?2SO3��H��0�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����ab�����иı������������| 1 |
| 2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com