
【题目】镍粉在CO中低温加热,生成无色挥发性液态Ni(CO)4,呈四面体构型。150℃时,Ni(CO)4分解为Ni和CO。则下列可作为溶解Ni(CO)4的溶剂是( )
A.水B.四氯化碳C.盐酸D.硫酸镍溶液
科目:高中化学 来源: 题型:
【题目】常温,下列溶液中各浓度关系不正确的是
A. 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液pH>7,则一定有:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
B. 1L0.1molL-1CuSO4·(NH4)2SO46H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-)
C. 0.1molL-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)≠c(HCO3-)+c(CO32-)+c(OH-)
D. 物质的量浓度分别为c1和c2的两种醋酸溶液,若其pH分别为a和a+1,则c1>10c2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人认为人体其实是一架缓慢氧化着的“高级机器”,人体在生命进程中也需要不断地补充“燃料”。按照这种说法,你认为人们通常摄入的下列物质中不能看成“燃料”的是( )
A. 淀粉 B. 脂肪 C. 水 D. 蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》“烧酒”条目:“自元时始创其法,用浓酒和糟入甑,蒸令气上,其清如水,味极浓烈,盖酒露也。”文中的“法”指( )
A.萃取B.蒸发C.蒸馏D.升华
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Na2O2可用作漂白剂和呼吸面具中的供氧剂.
(1)写出Na2O2作供氧剂的反应方程式________________________________________。
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。
步骤1:按图组装仪器(图中夹持仪器省略),检查气密性,装入药品;

步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象;
步骤3:……,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①盛装稀盐酸的仪器名称_________;B装置的作用是___________________________。
②步骤3在点燃C处酒精灯前必须进行的操作是________________。
③设置装置D的目的是_______________________。
④根据实验现象你得到的结论是______________________________(用化学方程式表示)。
⑤该实验设计中存在着明显不足之处,应该如何改进:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能成功的是( )
A. 苯与液溴反应(Fe作催化剂)制溴苯 B. 用金属钠检验乙醇中是否含有水
C. 乙烷能使酸性KMnO4溶液褪色 D. 苯能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中常见的金属防腐的方法很多。下列措施不能起到防腐作用的是( )
A. 健身器材刷油漆 B. 衣架和电线的外面包上一层塑料层
C. 在轮船船身上装上一定数量的铜块 D. 地下钢铁管道连接锌块
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】看如图完成下面的填空,写出电极反应式和总反应式. 
(1)Fe电极是(填“正”或“负”)极,其电极反应为 , 该反应是(填“氧化”或“还原”)反应;
(2)Cu电极是极,其电极反应为 , 该反应是反应.
(3)电池总反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理应用和处理元素化合物,在生产生活中有重要意义。尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
(1)以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
关于该反应的下列说法正确的是________(填字母序号)。
A.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.当容器中NH3的体积分数不再改变时,反应处于平衡状态
(2)尿素在一定条件下可将氮的氧化物还原为氮气。
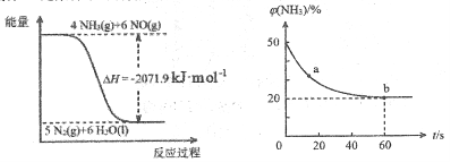
根据图像,结合(1)中信息,尿素还原NO(g)的热化学方程式是_____________________________________。
(3)密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+NH3(g)![]() CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com