
元素的性质呈现周期性变化的根本原因是()
A. 原子半径呈周期性变化
B. 元素的化合价呈周期性变化
C. 第一电离能呈周期性变化
D. 元素原子的核外电子排布呈周期性变化
考点: 元素周期律的实质.
分析: 根据随原子序数的递增,原子的结构呈现周期性的变化而引起元素的性质的周期性变化来解答.
解答: 解:A、因元素的原子半径是元素的性质,不能解释元素性质的周期性变化,故A错误;
B、因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故B错误;
C、因第一电离能呈周期性变化,则不能解释元素性质的周期性变化,故C错误;
D、因原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故D正确;
故选:D.
点评: 本题考查元素周期律的实质,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键,并注意不能用元素本身的性质来解释元素性质的周期性变化.


科目:高中化学 来源: 题型:
下列说法正确的是()
A. 能电离出H+的化合物叫做酸
B. 实验测得1mol某气体体积为22.4L,测定条件一定是标准状况
C. 摩尔是七个基本物理量之一
D. 用树状分类法可以将化合物分类为酸、碱、盐和氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
请完成下列填空:
(1)同温同压下等体积的SO2和SO3中,所含原子数之比为 .
(2)中和100mL 0.1mol/L的稀硫酸,需NaOH的质量为
(3)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g•mol﹣1,则:
①该气体在标准状况下的体积为
②该气体溶于水后形成V L溶液(不考虑反应),其溶液的物质的量浓度 L﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列化学反应热现象,正确的说法是()
A. 放热的反应发生时不必加热
B. 化学反应一定有能量变化
C. 化学反应一般地说,吸热反应需要加热后才能发生
D. 化学反应热效应数值与反应物质多少无关
查看答案和解析>>
科目:高中化学 来源: 题型:
把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸根,则原混合溶液中钾离子的浓度为()
A. 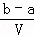 mol/L B.
mol/L B. 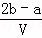 mol/L C.
mol/L C. 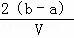 mol/L D.
mol/L D. 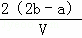 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
除去NaCl中含有的Ca2+、Mg2+、SO42﹣、HCO3﹣等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl,加入试剂合理的操作顺序是()
A. ①②③④ B. ③①②④ C. ④②①③ D. ③②①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com