
Mg(OH)2的溶度积是1.2×10-11(291K),在该温度下,下列pH值中,哪一个是Mg(OH)2饱和溶液的pH值.
A. 10.2 B. 7 C. 5 D. 3.2
科目:高中化学 来源: 题型:
A.Mg(OH)2的溶度积大于MgCO3的溶度积,且在水中发生了沉淀转化
B.Mg(OH)2的溶度积小于MgCO3的溶度积,且在水中发生了沉淀转化
C.MgCO3电离出的![]() 发生水解,使水中OH-浓度减小,对Mg(OH)2的沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀
发生水解,使水中OH-浓度减小,对Mg(OH)2的沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀
D.MgCO3电离出的![]() 发生水解,使水中OH-浓度增大,对Mg(OH)2的沉淀溶解平衡而言,Qc>Ksp,生成Mg(OH)2沉淀
发生水解,使水中OH-浓度增大,对Mg(OH)2的沉淀溶解平衡而言,Qc>Ksp,生成Mg(OH)2沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中提取镁的工业流程如下图所示:

回答下列问题。
⑴用贝壳而不从异地山中开凿石灰石的原因是______________________________。
⑵母液中含有MgCl2,写出反应池1的离子方程式_________________________。
⑶反应池1中,加入Ca(OH)2,使溶液的pH为11时,认为Mg2+沉淀完全[c(Mg2+)<1×10-5mol·L-1],则Mg(OH)2的溶度积约为_______________________。
⑷干燥塔中,在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是_______________________________________________________________。
⑸电解槽中先得到的是镁的蒸气,镁蒸气可以在下列_____(填编号)气体氛围中冷却。
A.空气 B.氧气 C.水蒸气 D.氢气
⑹镁可用于生产金属钛,主要步骤有:①在高温下,向金红石(主要成分TiO2)与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体;②在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛。写出上述两步反应的化学方程式。
反应①:____________________________________________________________;
反应②:____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013届山东省青州一中高三10月阶段测试化学试卷(带解析) 题型:填空题
(10分)从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题:
(1)流程甲通入过量CO2后生成沉淀F的离子反应方程式为______________________________________。
(2流程乙加入烧碱溶解SiO2的化学反应方程式____________________。
(3)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途____________________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱至达到沉淀溶解平衡,测得pH=12,则此温度下残留在溶液中的c(Mg2+)=________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省高安中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(18分)按要求回答下列问题
(1)用标准NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作中会导致实验结果偏低的是 (填序号 )
①碱式滴定管用蒸馏水洗净后没有用标准液润洗
②用酸式滴定管加待测液时,刚用蒸馏水洗净后的滴定管未用待测液润洗
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确
(2)某课外活动小组同学用如图甲装置进行实验,试答下列问题: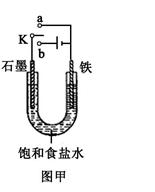
①若开始时开关K与a连接,则铁发生电化学腐蚀中的 腐蚀。
②若开始时开关K与b连接,则总反应的离子方程式为 。
(3)已知:铅蓄电池总的化学方程式为:Pb+PbO2 +2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
①铅蓄电池在放电时负极反应为 ,
②铅蓄电池在充电时阳极反应为 ;
③如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H2SO4 mol。
(4)常温下,如果取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,求出混合液中下列算式的精确计算结果(填具体数字):
c(OH-)-c(HA)= ___________ mol/L。
(5)在Cl-、Al3+、HSO4-、K+、HS-五种离子中,只能水解不能电离的离子是 ,只能电离不能水解的离子是 ,既能电离又能水解的离子是 ,写出能水解离子的水解离子方程式 , 。
(6)已知25℃时,Mg(OH)2的溶度积常数Ksp = 5.6×10-12,测得某溶液的pH = 13,则此温度下溶液中的c(Mg2+) = ____________________。
查看答案和解析>>
科目:高中化学 来源:2010年银川二中高考预测(综合题)化学卷 题型:填空题
白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下: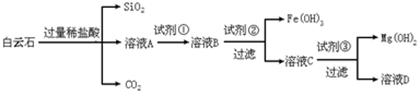
实验过程中需要的数据见下表:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
| A.KMnO4 | B.Cl2 | C.MgO | D.CaO |
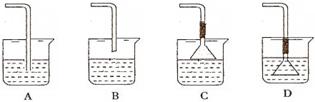
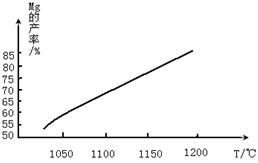
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com