
��֪��ӦAsO43����2I����2H�� AsO32����I2��H2O�ǿ��淴Ӧ�������ͼװ��(C1��C2��Ϊʯī�缫)���ֱ��������������
AsO32����I2��H2O�ǿ��淴Ӧ�������ͼװ��(C1��C2��Ϊʯī�缫)���ֱ��������������
��.��B�ձ�����μ���Ũ����
��.��B�ձ�����μ���40% NaOH��Һ
������ֵ�����ָ�������ƫת��
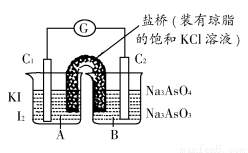
�ݴˣ������ж���ȷ����(����)
A�������������У�C1Ϊ����
B�������������У������е�K������B�ձ���Һ
C�������������У�C2���Ϸ����ķ�ӦΪ��AsO43����2H����2e��=AsO33����H2O
D�������������У�C1���Ϸ����ķ�ӦΪ��2I��=I2��2e��
 �ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�
�ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д� ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 8-1 ������ʵĵ���ƽ����ϰ���������棩 ���ͣ������
������ʵ�����������õ���Ⱥ͵���ƽ�ⳣ����ʾ����1�dz����¼�������ĵ���ƽ�ⳣ��(Ka)������ĵ���ƽ�ⳣ��(Kb)����2�dz����¼�����()������ܶȻ�����(Ksp)��
��1
���� | ����ƽ�ⳣ��(Ka��Kb) |
CH3COOH | 1.8��10��5 |
HNO2 | 4.6��10��4 |
HCN | 5��10��10 |
HClO | 3��10��8 |
NH3��H2O | 1.8��10��5 |
��2
��()���� | �ܶȻ�����(Ksp) |
BaSO4 | 1��10��10 |
BaCO3 | 2.6��10��9 |
CaSO4 | 7��10��5 |
CaCO3 | 5��10��9 |
��ش��������⣺
(1)��1�������������У�������������________________(�û�ѧʽ��ʾ)��������ʹ������Һ��CH3COOH�ĵ���̶��������볣������IJ�����________(�����)��
A�������¶�
B����ˮϡ��
C����������CH3COONa����
D��������������
(2)CH3COONH4��ˮ��Һ��________(ѡ������������������������������)��������_______________����Һ�и�����Ũ�ȴ�С��ϵ��______��
(3)���ʵ���֮��Ϊ1��1��NaCN��HCN�Ļ����Һ����pH>7������Һ������Ũ�ȴӴ�С������Ϊ______________________��
(4)��ҵ�г���BaSO4ת��ΪBaCO3���ٽ����Ƴɸ��ֿ����Եı���(��BaCl2)�������������ñ��͵Ĵ�����Һ����BaSO4��ĩ�������ϲ��䴿����BaSO4ת��ΪBaCO3������������BaSO4����Һ���ڸ�����Һ�мӴ����ĩ�����Ͻ��裬ΪʹSO42�����ʵ���Ũ�Ȳ�С��0.01 mol��L��1������Һ��CO32�����ʵ���Ũ��Ӧ��________ mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 7-2 ��ѧ��Ӧ�ķ��������ϰ���������棩 ���ͣ�ѡ����
��ͬ�¶��£��������ȵ����������ܱ������з������淴Ӧ��N2(g)��3H2(g) 2NH3(g)����H����92.4 kJ��mol��1��
2NH3(g)����H����92.4 kJ��mol��1��
ʵ������ʼ��ƽ��ʱ���й��������±���
������� | ��ʼʱ���������ʵ���/mol | ƽ��ʱ��Ӧ�е������仯 | ||
N2 | H2 | NH3 | ||
�� | 1 | 3 | 0 | �ų�����a kJ |
�� | 2 | 3 | 0 | �ų�����b kJ |
�� | 2 | 6 | 0 | �ų�����c kJ |
����������ȷ����(����)
A���ų�������ϵ��a<b<92.4
B�����������ڷ�Ӧ��ƽ�ⳣ������>��>��
C����ƽ��ʱ�����������������>��
D��N2��ת���ʣ���>��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 7-1 ��ѧ��Ӧ������ϰ���������棩 ���ͣ�ѡ����
Ϊ�˽�һ���о�����ͭ�����������������ʵ�Ӱ�죬ijͬѧ��������һϵ��ʵ�顣�������������Լ���һ�������Ϻֱ�����ĸ�ʢ�й���Zn���ķ�Ӧƿ(�ס��ҡ�������)�У��ռ����������壬��¼�ռ���ͬ�������������ʱ�䡣
ʵ�� �Լ�/mL | �� | �� | �� | �� |
4 mol/L H2SO4 | 20 | V1 | V2 | V3 |
����CuSO4��Һ | 0 | 2.5 | V4 | 10 |
H2O | V5 | V6 | 8 | 0 |
����˵����ȷ����(����)
A��ʵ��ײ������ݵ�������� ������B��V1<V2<V3<20
C��V4��V5��10 ������D��V6��7.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 6-3 ԭ��ؽ����ĸ�ʴ��������ϰ���������棩 ���ͣ������
��ͼ��ʾ����ʯī�缫����Ȼ�ͭ��Һ���������Ͽ�֪��CuCl42���Ի�ɫ���Ȼ�ͭ��Һ������ɫ�����ɫ���������ͬŨ�ȷֱ�Ϊ0.01 mol/L��0.05 mol/L��0.1 mol/L��0.5 mol/L���Ȼ�ͭ��Һ�м���NaCl�����ͣ��Աȷ��֣���Һ����ɫ�ɻ���ɫ������ɫת�䡣
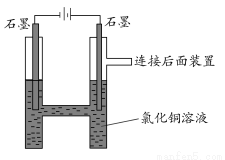
��ش��������⣺
(1)�����ϵ������________ɫ��������������________________��
(2)д���������ӷ���ʽ��________________��
(3)ʵ��ʱ��װ����������Һ��ɫ������ɫ��Ϊ����ɫ��ԭ����________��
(4)ȡ��������ʯī�������ֱ�����dz��ɫ���壬�����ʵ��̽����dz��ɫ����ijɷ֣�
____________________________________________________��
(5)ΪʲôҪ������Ӻ����װ�ã�
______________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 6-3 ԭ��ؽ����ĸ�ʴ��������ϰ���������棩 ���ͣ�ѡ����
ͭ������í������������ʴԭ����ͼ��ʾ�������й�˵���У�����ȷ����(����)
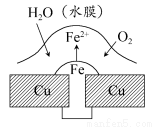
A���˹�����ͭ��������ʴ
B���˹����е��Ӵ�Fe����Cu
C��������ӦʽΪ��2H����2e��=H2��
D���˹����л��漰��Ӧ��4Fe(OH)2��2H2O��O2=4Fe(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 6-2 ԭ��ء������Ļ�ѧ��Դ��ϰ���������棩 ���ͣ������
����������ԭ��Ӧ��2Ag��(aq)��Cu(s)=Cu2��(aq)��2Ag(s)��Ƶ�ԭ�����ͼ��ʾ����������Ϊ����?����KNO3���š���ش��������⡣(����)
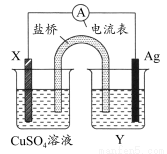
(1)�缫X�IJ�����________���������ҺY��________��
(2)���缫Ϊ��ص�________����д�����缫�ĵ缫��Ӧʽ��
���缫��_________________________________________________��
X�缫��___________________________________________________��
(3)���·�У������Ǵ�________�缫����________�缫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 6-1 ��ѧ��Ӧ�е���ЧӦ��ϰ���������棩 ���ͣ������
(1)����ɴ��ϵ�����ȼ�ϵ�أ����ط�ӦΪ��2H2��O2=2H2O����д���������Һ��Ϊ����ʱ��������Ӧʽ��______________��
(2)��֪4 g����������ȼ������CO2(g)��H2O(l)ʱ���ų�Q kJ��������д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ��______________________��
(3)��֪�����Ȼ�ѧ����ʽ��
��Fe2O3(s)��3CO(g)=2Fe(s)��3CO2(g)����H����Q1 kJ/mol
��3Fe2O3(s)��CO(g)=2Fe3O4(s)��CO2(g)����H����Q2 kJ/mol
��Fe3O4(s)��CO(g)=3FeO(s)��CO2(g)����H����Q3 kJ/mol
���ø�˹���ɼ�����FeO(s)��CO(g)=Fe(s)��CO2(g)���ʱ���H��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ�ս̰��ܸ�ϰ 5-1 �����ԭ�ӽṹ����ʶ��ϰ���������棩 ���ͣ�ѡ����
ijԪ�ص�һ��ͬλ��X��ԭ��������ΪA����N�����ӣ�����1Hԭ�����HmX���ӡ���ag HmX���������ӵ����ʵ�����( )
A�� (A��N��m) mol B��
(A��N��m) mol B��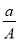 (A��N) mol
(A��N) mol
C��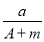 (A��N) mol D��
(A��N) mol D��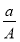 (A��N��m) mol
(A��N��m) mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com