
| A、KI氧化剂 |
| B、KIO3还原剂 |
| C、I2既是氧化产物又是还原产物 |
| D、该反应是复分解反应 |


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25°C时,pH=3的1.0L NaHSO3溶液中,含Na+数目为0.001 NA |
| B、0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| C、2.3g甲苯和丙三醇的混合物中,含氢原子数目为0.2 NA |
| D、标准状况下,22.4L乙醇中含有的氧原子数为1.0NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、+1164.1kJ?mol-1 |
| B、-1641.0kJ?mol-1 |
| C、-259.7kJ?mol-1 |
| D、-519.4kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钙和醋酸 CaCO3+2H+═Ca2++H2O+CO2↑ | ||||
| B、碳酸氢钙溶液和足量氢氧化钠溶液 Ca2++HCO3-+OH-=CaCO3↓+H2O | ||||
| C、铜和稀硝酸反应 Cu+4H++NO3?═Cu2++NO↑+2H2O | ||||
D、硫酸铵溶液和氢氧化钠溶液共热 NH4++OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烷和氯气光照下制取纯净的氯乙烷 |
| B、用分液漏斗分离环己烷和水的混合液体 |
| C、用浓氨水洗涤做过银镜反应的试管 |
| D、在苯和溴水的混合物中加入铁粉制取溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
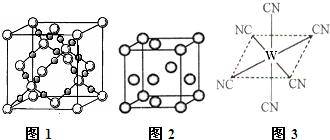
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com