
| A. | Zn2+、Fe2+和Cu2+ | B. | Zn2+、Fe3+和Cu2+ | C. | Fe2+和Zn2+ | D. | Cu2+ 和Zn2+ |
分析 n(CuSO4)=$\frac{16.0g}{160g/mol}$=0.1mol,n[Fe2(SO4)3]=$\frac{20g}{400g/mol}$=0.05mol,n(Zn)=$\frac{9.75g}{65g/mol}$=0.15mol,氧化性强弱顺序是Fe3+>Cu2+,根据转移电子守恒确定溶液中存在的离子,据此分析解答.
解答 解:n(CuSO4)=$\frac{16.0g}{160g/mol}$=0.1mol,n[Fe2(SO4)3]=$\frac{20g}{400g/mol}$=0.05mol,n(Zn)=$\frac{9.75g}{65g/mol}$=0.15mol,氧化性强弱顺序是Fe3+>Cu2+,Zn完全反应转移电子物质的量=0.15mol×2=0.3mol,如果Fe3+完全反应,转移电子物质的量=2n[Fe2(SO4)3]×1=2×0.05mol×1=0.1mol,铜离子完全反应转移电子物质的量=0.1mol×2=0.2mol,Fe3+、Cu2+完全反应转移电子物质的量=(0.1+0.2)mol=0.3mol,所以Zn完全溶解,溶液中离子为Fe2+和Zn2+,
故选C.
点评 本题考查化学方程式有关计算,为高频考点,侧重考查学生分析计算能力,利用转移电子守恒确定溶液中参加反应的离子,明确离子反应先后顺序是解本题关键,题目难度中等.


 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源: 题型:选择题
| A. | 向NaAlO2溶液通入过量的CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+2I-+8H+═3Fe2++I2+4H2O | |
| C. | 用FeS除去工业废水中的Hg2+:Hg2++S2-═HgS↓ | |
| D. | 向饱和的Ca(OH)2溶液中滴加过量NaHCO3溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
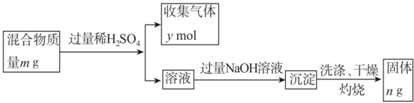
| W | X | Y | Z | |
| 结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1molNa与O2在一定条件下生成Na2O和Na2O2混合物时,失去电子数为0.2NA | |
| B. | 50mL 12mol•L-1浓盐酸与足量二氧化锰加热反应,生成Cl2的分子数为0.15NA | |
| C. | 常温下,100mL 1mol•L-1Na2CO3溶液中阴离子总数等于0.1NA | |
| D. | 标准状况下,6.72LCO2中所含的共用电子对数为1.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 式量为30的碳、氢、氧组成的化合物无同分异构体 | |
| B. | 式量为128的烃的分子式不一定是C9H20 | |
| C. | 烃的式量可以是偶数,也可以是奇数 | |
| D. | 有机物分子中,H原子数可以是偶数,也可以是奇数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 处理锅炉水垢的CaSO4,可先用Na2CO3溶液处理,再用酸去除 | |
| B. | 向TiCl4中加入大量的水,同时加热,可以制备纳米材料制备TiO2 | |
| C. | AlCl3溶液蒸干灼烧得不到AlCl3,而用SOCl2与AlCl3•6H2O混合共热可得无水AlCl3 | |
| D. | 铵态氮肥不可与草木灰同时使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
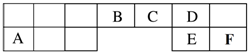
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com