
下列说法正确的是 ( )
A.O2和O3互为同位素,化学性质相似
B.水是一种非常稳定的化合物,这是由于氢键所致
C.分子晶体中一定存在分子间作用力,但可能没有共价键
D.将标准状况下22.4 L 氨气溶于1 L水配成溶液,可得1 mol·L-1的氨水
科目:高中化学 来源:2016届湖北省高三5月模拟三理综化学试卷(解析版) 题型:选择题
下列说法中不正确的是
A.无机非金属材料中不可能含有金属元素
B.铝盐、铁盐有净水作用,向浑浊的水中加入少量明矾或硫酸铁溶液,搅拌,过一段时间,水的底部会出现很多絮状不溶物,水变澄清透明
C.氯化物在化学工业领域有重要应用,例如SiCl4、GeCl4、TiCl4分别是制取高纯硅、锗和钛的重要中间物质
D.地球上存在的天然二氧化硅形态有结晶形和无定形两大类统称硅石
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三考前热身理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】硼和氮元素在化学中有很重要的地位,回答下列问题:
(1)基态硼原子核外电子有________种不同的运动状态,基态氮原子的价层电子排布图为_________。预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2]。(CH3)2NNH2中N原子的杂化方式为_________。
(2)化合物H3BNH3是一种潜在的储氢材料,可利用化合物B3N3H6通过如下反应制得:3CH4+2B3N3H6+6H2O=3CO2+6H3BNH3
①H3BNH3分子中是否存在配位键_______________(填“是”或“否”),B、C、N、O的第一电离能由小到大的顺序为___________________。
②与B3N3H6互为等电子体的分子是_____________(填一个即可),B3N3H6为非极性分子,根据等电子原理写出B3N3H6的结构式____________________________。
(3)“嫦娥五号”探测器采用太阳能电池板提供能量,在太阳能电池板材料中除单晶硅外,还有铜,铟,镓,硒等化学物质,回答下列问题:
①SeO3分子的立体构型为_____________。
②金属铜投入氨水或H2O2溶液中均无明显现象,但投入氨水与H2O2的混合溶液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子反应方程式为 。
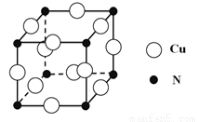
③某种铜合金的晶胞结构如图所示,该晶胞中距离最近的铜原子和氮原子间的距离为 pm,则该晶体的密度为_________________(用含a的代数式表示,设NA为阿伏伽德罗常数的值)。
pm,则该晶体的密度为_________________(用含a的代数式表示,设NA为阿伏伽德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前模拟理综化学试卷(解析版) 题型:填空题
在 2 L 容积不变的密闭容器内,800 ℃时反应 2NO(g)+O2 (g) 2NO2 (g)体系中,n(NO)随时间的变化如下表:
2NO2 (g)体系中,n(NO)随时间的变化如下表:

(1)用O2的反应速率表示 0~2s 内该反应的平均反应速率 v=________________。若上述反应在850 ℃下进行,反应2s时 n(NO)=0.009 mol,并且不再随时间而改变,则该反应是__________热反应。
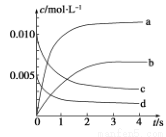
(2)图中表示NO2浓度变化的曲线是__________(填字母)。
(3)能说明该反应已达到平衡状态的是________(填序号)。
A.v(NO2)=2v(O2)
B.容器内的压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内气体密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________(填序号)。
A.及时分离出NO2
B.适当升高温度
C.增大O2的浓度
D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前模拟理综化学试卷(解析版) 题型:选择题
在下列叙述仪器“0”刻度位置正确的是( )
A.在量筒的上端
B.在滴定管上端
C.在托盘天平刻度尺的正中
D.在托盘天平刻度尺的右边
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二6月月考化学试卷(解析版) 题型:选择题
一定量的乙醇在氧气不足的情况下燃烧,得到的CO2、CO和H2O的总质量为27.6g,若期中H2O的质量为10.8g,则CO的质量是
A.4.4g B.2.2g C.1.4g D.在2.2g和4.4g之间
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二6月月考化学试卷(解析版) 题型:选择题
化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1∶2∶2∶3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是


A.A分子属于酯类化合物,在一定条件下不能发生水解反应
B.A在一定条件下可与4 mol H2发生加成反应
C.与A属于同类化合物的同分异构体只有2种
D.符合题中A分子结构特征的有机物只有1种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二6月月考化学试卷(解析版) 题型:选择题
用0.2mol/L Na2SO3溶液32mL,还原含2×10-3 mol X2O72-的溶液,过量的Na2SO3用0.1mol/L KMnO4酸性溶液氧化(其中KMnO4被还原成Mn2+),共消耗KMnO4溶液1.6mL,则元素X在还原产物中的化合价是( )
A.+3 B.+4 C.+5 D.+6
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷(解析版) 题型:简答题
【化学——选修3:物质结构与性质】目前半导体生产展开了一场“铜芯片”革命——在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:

(1)基态铜原子的外围电子排布式为__________________,硫、氧元素相比,第一电离能较大的元素是________(填元素符号)。
(2)反应①、② 中均生成有相同的气体分子,该分子的中心原子杂化类型是____,其立体结构是______。
中均生成有相同的气体分子,该分子的中心原子杂化类型是____,其立体结构是______。
(3)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液 蓝色沉淀
蓝色沉淀 沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式 ___;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
沉淀溶解,得到深蓝色透明溶液。写出蓝色沉淀溶于氨水的离子方程式 ___;深蓝色透明溶液中的阳离子(不考虑H+)内存在的全部化学键类型有 。
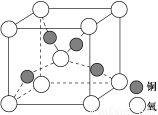
(4) 铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途,铜晶体中铜原子堆积模型为_____________;铜的某种氧化物晶胞结构如图所示,若该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞中铜原子与氧原子之间的距离为________pm。 (用含d和NA的式子表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com