
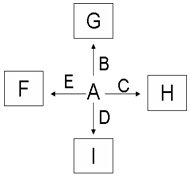
 如图中,A、B、C、D、E均为单质,A分别与B、C、D、E反应生成了相应的二元化合物G、H、I、F.已知①C+G B+H B+H可用于焊接钢轨,其中G为黑色磁性固体.
如图中,A、B、C、D、E均为单质,A分别与B、C、D、E反应生成了相应的二元化合物G、H、I、F.已知①C+G B+H B+H可用于焊接钢轨,其中G为黑色磁性固体.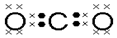 .
.分析 A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,
①反应C+G$\frac{\underline{\;高温\;}}{\;}$B+H能放出大量的热,该反应曾应用于铁轨的焊接,该反应为铝热反应,则C为Al,B为Fe,G为Fe2O3,H为Al2O3,
②I是一种常见的温室气体,则I为CO2,它和E可以发生反应:2E+I$\frac{\underline{\;点燃\;}}{\;}$2F+D,F中的E元素的质量分数为60%,则E为Mg,D为C,F为MgO,由图中转化可知,A为O2.
然后结合元素化合物知识及化学用语来解答.
解答 解:A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,
①反应C+G$\frac{\underline{\;点燃\;}}{\;}$B+H能放出大量的热,该反应曾应用于铁轨的焊接,G为黑色磁性固体,该反应为铝热反应,则C为Al,B为Fe,G为Fe3O4,H为Al2O3,
②I是一种常见的温室气体,则I为CO2,它和E可以发生反应:2E+I$\frac{\underline{\;点燃\;}}{\;}$2F+D,F中的E元素的质量分数为60%,则E为Mg,D为C,F为MgO,由图中转化可知,A为O2.
(1)单质A为O2.I为二氧化碳,其电子式为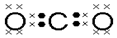 ,
,
故答案为:O2;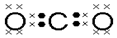 ;
;
(2)化合物G与足量稀盐酸反应的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O,
故答案为:Fe3O4+8H+═Fe2++2Fe3++4H2O;
(3)E在I中燃烧的化学方程为:2Mg+CO2 $\frac{\underline{\;点燃\;}}{\;}$ 2MgO+C,
故答案为:2Mg+CO2 $\frac{\underline{\;点燃\;}}{\;}$ 2MgO+C;
(4)C与过量NaOH溶液反应的化学方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 本题考查无机物的推断,注意利用铝热反应及温室效应气体、Mg与二氧化碳的反应为解答本题的突破口,熟悉Mg、Al及其化合物的性质及氧化还原反应即可解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 将w g a%的NaCl溶液蒸发掉$\frac{w}{2}$g水,得到2a%的NaCl溶液 | |
| B. | 将1Lc mol/L的硫酸溶液用4L水稀释,稀释后溶液的物质的量浓度等于0.2c mol/L | |
| C. | 标准状况下,将a L HCl气体溶于1 L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为$\frac{1000ad}{36.5a+22.4}$ | |
| D. | 将1.6 g CuSO4•5H2O晶体溶于水配成1L溶液,制得0.01 mol/L的CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与水反应(乙醇) | |
| B. | 乙烯与氯气反应(二氯乙烷) | |
| C. | 液溴与苯用溴化铁作催化剂反应(溴苯) | |
| D. | 等物质的量的氯气与乙烷在光照条件下反应(氯乙烷) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClCH2CH2OH | B. | OHC-O-CH2Cl | C. | ClCH2CHO | D. | HOCH2CH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
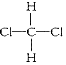 和
和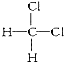
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,将1g乙炔溶于12g苯,所得混合物中含有的碳原子数为NA | |
| B. | 1 mol FeCl3完全水解转化为氢氧化铁胶体后生成NA个胶粒 | |
| C. | 标况下,11.2 L的HF所含分子数为0.5 NA | |
| D. | 133.5 g氯化铝固体中含有NA个铝离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
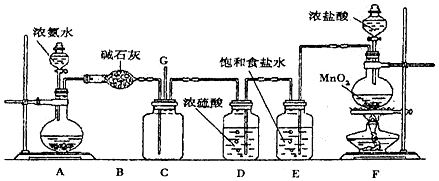
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
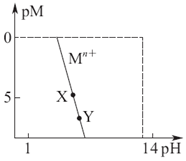 常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5 mol•L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )
常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5 mol•L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )| A. | Mn+开始沉淀的pH与起始溶液c(Mn+)无关 | |
| B. | 不同的金属沉淀完全时的pH相同 | |
| C. | 图中Y点与X点pKsp不相同 | |
| D. | Y点:pM=pKsp+npH-14n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com