

 的合成路线如图2:[( )内为反应类型,
的合成路线如图2:[( )内为反应类型, 内为目标产物]
内为目标产物] 内物质的结构简式:Ⅰ
内物质的结构简式:Ⅰ ,葡萄糖在乳酸菌的作用下生成C为乳酸,即CH3CHOHCOOH,由E能发生加聚反应可知C生成D的反应为消去反应,则D为CH2=CHCOOH,E为丙烯酸和乙醇发生酯化反应生成的酯,为CH2=CHCOOCH2CH3,F为
,葡萄糖在乳酸菌的作用下生成C为乳酸,即CH3CHOHCOOH,由E能发生加聚反应可知C生成D的反应为消去反应,则D为CH2=CHCOOH,E为丙烯酸和乙醇发生酯化反应生成的酯,为CH2=CHCOOCH2CH3,F为 ,由G合成
,由G合成 ,可以将CH3CH2OH发生消去反应生成Ⅰ为CH2=CH2,CH2=CH2再与溴加成得Ⅱ为BrCH2CH2Br,BrCH2CH2Br再发生水解得Ⅲ为HOCH2CH2OH,HOCH2CH2OH再氧化得OHCCHO,OHCCHO再氧化得Ⅳ为HOOCCOOH,HOOCCOOH与前面得到的HOCH2CH2OH发生缩聚反应即得
,可以将CH3CH2OH发生消去反应生成Ⅰ为CH2=CH2,CH2=CH2再与溴加成得Ⅱ为BrCH2CH2Br,BrCH2CH2Br再发生水解得Ⅲ为HOCH2CH2OH,HOCH2CH2OH再氧化得OHCCHO,OHCCHO再氧化得Ⅳ为HOOCCOOH,HOOCCOOH与前面得到的HOCH2CH2OH发生缩聚反应即得 ,据此答题.
,据此答题. ,葡萄糖在乳酸菌的作用下生成C为乳酸,即CH3CHOHCOOH,由E能发生加聚反应可知C生成D的反应为消去反应,则D为CH2=CHCOOH,E为丙烯酸和乙醇发生酯化反应生成的酯,为CH2=CHCOOCH2CH3,F为
,葡萄糖在乳酸菌的作用下生成C为乳酸,即CH3CHOHCOOH,由E能发生加聚反应可知C生成D的反应为消去反应,则D为CH2=CHCOOH,E为丙烯酸和乙醇发生酯化反应生成的酯,为CH2=CHCOOCH2CH3,F为 ,由G合成
,由G合成 ,可以将CH3CH2OH发生消去反应生成Ⅰ为CH2=CH2,CH2=CH2再与溴加成得Ⅱ为BrCH2CH2Br,BrCH2CH2Br再发生水解得Ⅲ为HOCH2CH2OH,HOCH2CH2OH再氧化得OHCCHO,OHCCHO再氧化得Ⅳ为HOOCCOOH,HOOCCOOH与前面得到的HOCH2CH2OH发生缩聚反应即得
,可以将CH3CH2OH发生消去反应生成Ⅰ为CH2=CH2,CH2=CH2再与溴加成得Ⅱ为BrCH2CH2Br,BrCH2CH2Br再发生水解得Ⅲ为HOCH2CH2OH,HOCH2CH2OH再氧化得OHCCHO,OHCCHO再氧化得Ⅳ为HOOCCOOH,HOOCCOOH与前面得到的HOCH2CH2OH发生缩聚反应即得 ,
, ,I为
,I为 ,
, ;
; ;
;| 催化剂 |
| △ |
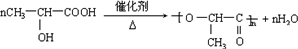 ,
,| 催化剂 |
| △ |
 ;
;

 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色透明的溶液:Na+、Al3+、Cl-、AlO2- |
| B、pH=1的溶液:Na+、NH4+、Cu2+、NO3- |
| C、与铝反应产生大量氢气的溶液:Na+、K+、Cl-、AlO2- |
| D、使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
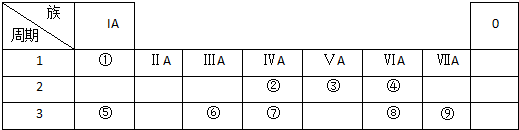
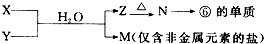
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物 质 | 除杂试剂 | 除杂和分离方法 | |
| A | 乙醇(水) | -- | 分液 |
| B | 铝粉(镁粉) | NaOH溶液 | 过滤 |
| C | CO2(CO) | O2 | 点燃 |
| D | CO(CO2) | NaOH溶液 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去乙烷中的少量乙烯的方法是将混合气体通过酸性高锰酸钾溶液 |
B、由CH2=CHCH3合成的聚合物为: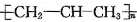 |
| C、分子式为C2H4O2的有机物都能与NaOH溶液反应 |
| D、丙烷的二溴取代产物比其三溴取代产物的种类少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com