
【题目】配制下列溶液时常需加入少量括号内的物质,其中不是为了抑制离子水解的是
A.FeSO4(Fe) B.SnCl2(HCl) C.FeCl3(HCl) D.NaAlO2(NaOH)
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置制取乙酸乙酯。回答下列问题:
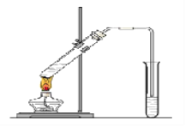
(1)写出制取乙酸乙酯的化学反应方程式: 。
(2)饱和碳酸钠溶液的主要作用是: 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是: 。
(4)应结束后,振荡试管b,静置。观察到的现象是 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是(填名称): 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法,用序号填空)。①溶解 ②裂解 ③分馏 ④裂化 ⑤干馏 ⑥蒸馏 ⑦过滤 ⑧电解 ⑨萃取
(1)将海水淡化 。
(2)从海水得到的无水MgC12中提取金属镁 。
Ⅱ、下图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。
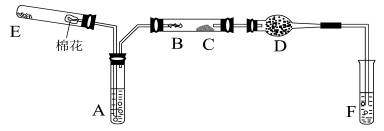
图中:A为无水乙醇(沸点为78℃),
B为绕成螺旋状的细铜丝或银丝,
C为无水CuSO粉末,
D为碱石灰,
F为新制的氢氧化铜悬浊液。
已知: 含—CHO的物质在加热条件下与新制的Cu(OH)2悬浊液反应生成砖红色沉淀.
(1)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) 。
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是_____________。
D处使用碱石灰的作是 。
(3) E处是一种纯净物,其反应方程式为 。
(4)写出乙醇发生催化氧化的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物中碳原子和氢原子个数比为3∶4,不能与溴水反应却能使酸性KMnO4溶液褪色。其蒸气密度是相同状况下甲烷密度的7.5倍。在铁存在时与溴反应,能生成两种一溴代物。该有机物可能是
A. CH≡C-CH3
B. ![]()
C. CH2=CHCH3
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。
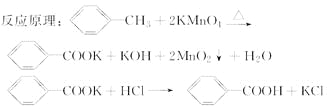
实验方法:一定量的甲苯和KMnO4溶液在100 ℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
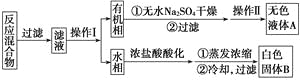
已知:苯甲酸分子量122,熔点122.4 ℃,在25 ℃和95 ℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为________,操作Ⅱ为________。
(2)无色液体A是________,定性检验A的试剂是________,现象是________。
(3)测定白色固体B的熔点,发现其在115 ℃开始熔化,达到130 ℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在完成表中内容。
序号 | 实验方案 | 实验现象 | 结果 |
① | 将白色固体B加入水中,加热溶解,________ | 得到白色晶体和无色滤液 | |
② | 取少量滤液于试管中,________ | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________ | ________ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 g产品,配成100 mL苯甲酸溶液,移取25.00 mL溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数的计算结果为________(保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中盛有2molNa2O2与2molNaHCO3,将其加热到150℃,经充分反应后,容器内残留的固体是( )
A.1molNa2CO3和2molNaOH B.2molNa2CO3和2molNaOH
C.2molNa2CO3和1molNa2O2 D.只有2molNa2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D四种元素的原子序数为A<B<C<D,且都小于18。A、B位于同周期,A元素的原子最外层电子数是次外层电子数的2倍,B元素的原子最外层电子数是次外层电子数的3倍。C、D同周期, C元素的原子半径在同周期中最大,D元素的原子最外层电子数比次外层电子数少1个。试推断:
(1)请写出A、B、C、D四种元素的元素符号:A________,B________,C________,D_______。
(2)画出D元素的离子结构示意图_______________。
(3)AB2中存在的化学键是 (离子键、共价键), CD的电子式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)微粒2311Na+ 中的质子数是_______,中子数是_______,核外电子数是_______。
(2)用电子式表示形成过程:H2S ;MgF2 。
(3)写出化学反应方程式:用四氧化三铁铝热法炼铁 ; 电解法冶炼铝 。
(4)有下列各组微粒或物质:
A.![]() C和
C和![]() C
C
B.CH3CH2CH2CH3和 CH3CH2CH(CH3)CH
C. 和
和 
D.CH3CH2CH2CH3和
①两种微粒互为同位素是__________;
②两种物质属于同系物的是__________;
③两种物质互为同分异构体的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH= -196.6kJ·mol-1
2SO3(g) ΔH= -196.6kJ·mol-1
2NO(g)+O2(g) ![]() 2NO2(g) ΔH= -113.0kJ·mol-1
2NO2(g) ΔH= -113.0kJ·mol-1
则反应NO2(g)+SO2(g) ![]() SO3(g)+NO(g)的ΔH= kJ·mol-1
SO3(g)+NO(g)的ΔH= kJ·mol-1
(2)一定条件下,将NO2与SO2以体积比2∶1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1molSO3的同时生成1mol NO
测得上述反应达平衡时NO2与SO2的体积比为5∶1,则平衡常数K=
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) ![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是: 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是: 。

(4)依据燃烧的反应原理,合成的甲醇可以设计如图(3)所示的原电池装置。
①该电池工作时,OH-向 极移动(填“正”或“负”)。
②该电池正极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com