
【题目】25℃时,向100 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.1 mol·L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图。下列说法不正确的是
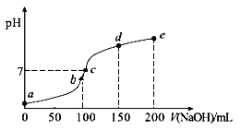
A. a点时溶液的pH<1
B. a点到b点的过程中,溶液的导电能力增强
C. c点关系式:c(NH4+)+c(Na+)=2c(SO42-)
D. b点时离子浓度大小顺序为: c(SO42-)=c(Na+)>c(NH4+)> c(H+)> c(OH-)
【答案】B
【解析】
a、b、c、d、e五个点,根据反应量的关系,b点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;c、d、e三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离.c点溶液呈中性,则溶液含有(NH4)2SO4、Na2SO4、NH3H2O三种成分。
A项、0.1molL-1NH4HSO4溶液中铵根离子水解溶液氢离子浓度大于0.1mol/L,a点时溶液的pH<1,故A正确;
B项、b点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4,溶液中溶质都是强电解质,溶液中离子浓度减小,导电性变化减小,故B错误;
C项、溶液中电荷守恒为:c(NH4+)+c(Na+)+c(H+)=2c(SO42-)+c(OH-),c点溶液呈中性,溶液中c(OH-)=c(H+),则c(NH4+)+c(Na+)=2c(SO42-),故C正确;
D项、b点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4,则b点时c(Na+)=c(SO42-),由于NH4+在溶液中水解,溶液呈酸性,故离子浓度大小顺序为c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故D正确。
故选B。


科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体, 一定条件下发生如下反应: 3A(g) ![]() B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )

A. 若 t1=15 s,则用 A 的浓度变化表示 t0~t1阶段的平均反应速率为 0.004 mol·L-1·s-1
B. t1时该反应达到平衡, A 的转化率为 60%
C. 该容器的容积为2 L,B的起始的物质的量为 0.02 mol
D. t0~t1 阶段, 此过程中容器与外界的热交换总量为 a kJ,该反应的热化学方程式为 3A(g)![]() B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)K2Cr2O7的水溶液中存在如下平衡:
Cr2O72-(aq)+ H2O(l)![]() 2CrO42-(aq)+ 2H+(aq),平衡常数表达式__________
2CrO42-(aq)+ 2H+(aq),平衡常数表达式__________
已知:(在水溶液中K2Cr2O7为橙红色,K2CrO4为黄色)往上述溶液中加入氢氧化钠,溶液呈___色;向已加入氢氧化钠的溶液中,再加入过量硫酸,溶液呈___________色。
(2)在KMnO4与H2C2O4反应中,可通过测定_________________来测定该反应的速率;写出酸性条件下KMnO4与H2C2O4(弱酸)反应,产生二氧化碳气体、水和Mn2+的离子反应方程式:__________________;此反应开始反应缓慢,随后反应迅速加快,其原因是______(填字母)
A.KMnO4溶液中的H+起催化作用
B.生成的CO2逸出,使生成物浓度降低
C.反应中,生成的Mn2+起催化作用
D.在酸性条件下KMnO4的氧化性增强
(3)为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
实验 序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
①该实验进行的目的是_____________
②表中Vx=_______mL,比较t1、t2、t3大小____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭恒容容器中,加入1molN2和3molH2发生反应:N2(g)+3H2(g)2NH3(g),下列叙述中能说明该反应达到平衡状态的是( )
A.![]() B.混合气体的密度保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变D.![]() :
:![]() :
:![]() :3:2
:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体必需元素之一,海洋植物含有丰富的碘元素。在实验中,从海藻里提取碘的流程如下:

(1)上图为海藻制碘的流程图。步骤①灼烧海藻时,除需要三脚架外,还需要用到的实验仪器是_____________________(从下列仪器中选出所需的仪器,用标号字母填写)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.冷凝管
(2)步骤③的名称为_____________,步骤⑤所需玻璃仪器除烧杯外还需___________________。
(3)步骤④中若不用氯气,可以选择滴加稀硫酸,再加入H2O2的方法,则反应的离子方程式为______________________________________。
(4)步骤⑤,可选择的有机试剂是___________。
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、甘油
(5)欲检验提取碘后的水溶液中是否含有单质碘的简单化学方法为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:NOx能与Na2O2反应;NO和NO2均能与酸性KMnO4溶液反应生成NO3ˉ和Mn2+。
I.用下图所示装置(略去夹持仪器)可制得少量亚硝酸钠(2NO+Na2O2=2NaNO2)。
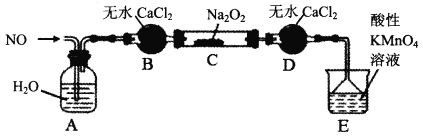
(1)B、D的仪器名称是________,D的作用是________。
(2)通NO前,需先通一段时间N2,目的是________,
(3)E中主要反应的离子方程式为________,
(4)常温下,测得实验前后C的质量差值为0.30g,则制得NaNO2________g。
Ⅱ.NO2和Na2O2都有较强氧化性,为探究NO2与Na2O2反应的产物,提出如下假设:
假设i.NO2氧化Na2O2;假设ii.Na2O2氧化NO2。
甲同学设计如图所示实验装置:

请回答下列问题:
(5)单向阀在实现气体单向流通的同时,还有一个作用是___________。
(6)待试管G中收集满气体,向试管G中加入适量Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃,甲同学据此认为假设i正确。乙同学认为该装置不能达到实验目的,为达到实验目的,应在F、G之间增加一个M装置,M中应盛装__________(可供选择的试剂:碱石灰,浓硫酸饱和氯化钠溶液);乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失,带火星的木条未复燃。得到结论:假设ⅱ正确。
请做出正确判断,写出NO2和Na2O2反应的化学方程式__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中说明NH3既有还原性,又有碱性的是( )
A. 4NH3+5O2![]() 4NO+6H2O B. NH3+HNO3=NH4NO3
4NO+6H2O B. NH3+HNO3=NH4NO3
C. 8NH3+3Cl2=N2+6NH4Cl D. 2NH3+3CuO![]() 3Cu+N2+3H2O
3Cu+N2+3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com