
| A、反应物总能量等于生成物总能量 |
| B、反应物总能量高于生成物总能量 |
| C、反应物总能量低于生成物总能量 |
| D、反应物总能量和生成物总能量的大小关系应视具体反应而定 |
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
| A、同时改变两个变量来研究反应速率的变化,能更快得出有关规律 |
| B、对于同一个化学反应,无论是正反应还是逆反应,其反应的焓变相同 |
| C、根据11-17号元素最高价氧化物对应水化物的酸碱性递变规律,推出同周期元素的金属性、非金属性递变规律 |
| D、从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a>b | B、a<b |
| C、a=b | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+,Na+,Cl-,NO3- |
| B、Cu2+,NO3-,OH-,HCO3- |
| C、CO32-,OH-,Cl-,K+ |
| D、NH4+,H+,Cl-,Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10℃20 mL 3 mol?L-1的X溶液 |
| B、20℃30 mL 2 mol?L-1的X溶液 |
| C、20℃10 mL 4 mol?L-1的X溶液 |
| D、10℃10 mL 2 mol?L-1的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知某温度下CH3COOH的电离常数K=1.6×10-5.该温度下向20mL 0.01mol?L-1CH3COOH溶液中逐滴加入0.01mol?L-1KOH溶液,其pH变化曲线如图所示(忽略温度变化).请回答下列有关问题:
已知某温度下CH3COOH的电离常数K=1.6×10-5.该温度下向20mL 0.01mol?L-1CH3COOH溶液中逐滴加入0.01mol?L-1KOH溶液,其pH变化曲线如图所示(忽略温度变化).请回答下列有关问题: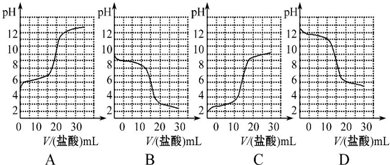
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com