
��9�֣��±���ʵ�����Ʊ�������й����ݣ�
��� | ʵ������ | ʵ��ԭ�� | ���巢��װ�� |
�� | �Ʊ����� | H2O2��O2 | |
�� | �Ʊ����� | NH4Cl��NH3 | |
�� | �Ʊ����� | HCl��Cl2 |
��1�������������Ʊ�ԭ���У����Ʊ����̿�������ѡ����ʵ�����������ʵ�ֵ��� ��������Ļ�ѧʽ����ͬ�����ӷ�Ӧԭ���������Բ�ͬ����������������� ��
��2�����ݱ�������ʵ��ԭ����������װ����ѡ����ʵ����巢��װ�ã������������ϱ��еĿո��С�
��3��ijѧϰС�����������ͼʵ�飬����������ͨ������װ������֤���������ʣ�
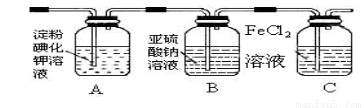
��ͨ��������A�е������� ��
����ʵ��װ�ô��ڵ�����ȱ���� ��
��Cװ���з�����Ӧ�����ӷ���ʽΪ: ��
(9�֣�ÿ��1��)
��1��Cl2 �� NH3
��2���� �� �� �� ����
��3������Һ��Ϊ��ɫ����β������װ�á���2Fe2+ �� Cl2 == 2Fe3+ + 2Cl����2�֣�
��������
�����������1�� ��1�� ��������������������������ԭ��Ӧ�����ư����Ǹ��ֽⷴӦ������ѡ����ʵ�����������ʵ�ֵ��Ǣ����������ӷ�Ӧԭ���������Բ�ͬ����������������Ǣ��ư�������2�� ����������Һ��������ϲ�����������Ӧѡװ�â������ư����Ǽ��ȹ�������������Ӧѡװ�â���������Һ�������������Ȼ���������Ӧѡװ�â�������3�� ͨ��������A�з�����ӦCl2+2KI=I2+2KCl,I2�����۱�����B�з���Cl2+SO32-+H2O=SO42-+2Cl-+2H+��C�з���2Fe2+ �� Cl2 == 2Fe3+ + 2Cl���������ж�������ʵ��װ����β������װ�ã�����ɿ�����Ⱦ��
���㣺�����Ʊ�ʵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ��г�����������ѧ�ڽ�ѧ������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�ʹ�ò��漰��ѧ�仯����
A������������ˮ�� B��Һ�����������
C��������ʴ���� D����ʯ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʦ���и������Ĵ�ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���У�����ȷ����
A��������Ԫ���У�����������������Ӳ���������Ԫ�ع���3��
B����������Ԫ�ص����Ӱ뾶��С�Ƚϣ�S2->Cl->Na+>Mg2+>Al3+
C���ձ��˵�վ�ͷų���131I��132I��133I����ͬ��������
D����ͬ�����£��ⶨͬŨ�ȵ�Na2CO3��Һ��Na2SO4��Һ��pH���ɱȽ�C��S�ķǽ�����ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ����ʽ�ɼ���������Ԫ�ؼ��仯��������ʡ���֪:
������ԭ��Ӧ��2FeCl3+2HI��2FeCl2+I2+2HCl��2Co��OH��3+6HCl��2CoCl2+Cl2��+6H2O��
2Fe��OH��2+I2+2KOH��2Fe��OH��3+2KI��3I2+6KOH��5KI+KIO3+3H2O
���ֽⷴӦ��2HSCN+K2CO3��2KSCN+CO2��+H2O�� KCN+CO2+H2O��HCN+KHCO3
�ȷֽⷴӦ��4NaClO3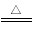 NaCl+NaClO4��NaClO4
NaCl+NaClO4��NaClO4 NaCl+2O2��
NaCl+2O2��
����˵������ȷ��:
A�����ԣ�ˮ��Һ): HSCN��H2CO3��HCN
B����ԭ��(������Һ): Fe��OH��2��I2��KIO3
C�����ȶ���: NaCl��NaClO4��NaClO
D��������(������Һ): I2��FeCl3��Co��OH��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ƶ���ȷ����
A��SiO2����NaOH��Һ��HF��Һ��Ӧ������SiO2������������
B��Na2O��Na2O2���Ԫ����ͬ���������������Ӹ�����Ҳ��ͬ
C��CO��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ�����
D��������ˮ�����ԣ������еμ�������ɫʯ����Һ���������Һ�ʺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ����1�¼�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
Na2CO3ˮ��Һ�д���CO2-3+H2O HCO-3+OH-ƽ�⡣����˵������ȷ����
HCO-3+OH-ƽ�⡣����˵������ȷ����
A��ϡ����Һ��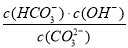 ����
����
B��ͨ��CO2����ҺpH��С
C�������¶ȣ���ƽ�ⳣ������
D������NaOH���壬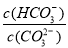 ��С
��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ����1�¼�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ƶ���ȷ����
A��SiO2 ���������������NaOH��Һ��Ӧ
B��Na2O��Na2O2���Ԫ����ͬ���� CO2��Ӧ����Ҳ��ͬ
C��CO��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ�����
D��������ˮ�����ԣ������еμ�������ɫʯ����Һ���������Һ�ʺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ����12��ѧ����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ���¶��£�������X������Y��0.16mol���� 10L�����ܱ������У�������Ӧ
X(g) + Y(g)  2Z(g) ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H < 0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t /min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A����Ӧǰ2min��ƽ������v(Z) =4.0��10-3mol/(L?min)
B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv(��) > v(��)
C�����¶��´˷�Ӧ��ƽ�ⳣ��K=1.44
D�������������䣬�ٳ���0.2molZ��ƽ��ʱX�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ����ʮУ���н̸Ĺ�ͬ�������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��7.8gþ���Ͻ���ȫ����������ϡ���ᣬ������״���µ�����8.96L����������Һ�м���������ϡ��ˮ�����ˣ�ϴ�ӣ�����������������ù�������Ϊ
A��14.2g B��21.4g C��5.8g D��4g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com