
·ÖĪö £Ø1£©øł¾Żn=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$½įŗĻĪļÖŹµÄ¹¹³É¼ĘĖć£»
£Ø2£©øł¾Żn=$\frac{m}{M}$¼ĘĖćĒāŃõ»ÆÄʵÄĪļÖŹµÄĮ棬ŌŁøł¾Żc=$\frac{n}{V}$¼ĘĖćČÜŅŗĪļÖŹµÄĮæÅØ¶Č£¬ČÜŅŗŹĒ¾łŌČµÄ£¬Č”³ö10mLČÜŅŗµÄÅضČÓėŌČÜŅŗÅضČĻąµČ£¬½«øĆ10mLČÜŅŗ¼ÓĖ®Ļ”ŹĶµ½100mL£¬ČÜÖŹ²»±ä£¬ÅضČĪŖŌĄ“µÄ$\frac{1}{10}$£»
£Ø3£©¢Łøł¾ŻM=¦ŃVmæÉÖŖ£¬ĻąĶ¬Ģõ¼žĻĀĘųĢåĆܶČÓėĦ¶ūÖŹĮæ³ÉÕż±Č£»
¢ŚĮ½øöČŻĘ÷ÖŠĘųĢåĆܶČĻąµČ£¬Ōņŗ¬ÓŠµÄĘųĢåµÄÖŹĮæĻąĶ¬£¬ČŻĘ÷ÖŠŃ¹ĒæÓėĘųĢåµÄĪļÖŹµÄĮæ³ÉÕż±Č£®
½ā“š ½ā£ŗ£Ø1£©n£ØOH-£©=$\frac{3.01”Į1{0}^{23}}{6.02”Į1{0}^{23}/mol}$=0.5mol£¬m£ØOH-£©=0.5mol”Į17g/mol=8.5g£¬ŗ¬ÓŠµē×ÓµÄĪļÖŹµÄĮæĪŖ0.5mol”Į10=5mol£¬n£ØNH3£©=$\frac{8.5g}{17g/mol}$=0.5mol£¬
¹Ź“š°øĪŖ£ŗ8.5g£»5mol£»0.5£»
£Ø2£©4g NaOHµÄĪļÖŹµÄĮæĪŖ$\frac{4g}{40g/mol}$=0.1mol£¬ČÜÓŚĖ®Åä³É250mLČÜŅŗ£¬“ĖČÜŅŗÖŠNaOHµÄĪļÖŹµÄĮæÅضČĪŖ$\frac{0.1mol}{0.25L}$=0.4mol/L£¬ČÜŅŗŹĒ¾łŌČµÄ£¬Č”³ö10mLČÜŅŗµÄÅضČÓėŌČÜŅŗÅضČĻąµČ£¬Č”³ö10mLČÜŅŗÖŠNaOHµÄĪļÖŹµÄĮæ=0.01L”Į0.4mol/L=0.004mol£¬½«øĆ10mLČÜŅŗ¼ÓĖ®Ļ”ŹĶµ½100mL£¬Ļ”ŹĶŗóČÜŅŗÖŠNaOHµÄĪļÖŹµÄĮæÅضČĪŖ$\frac{0.004mol}{0.1L}$=0.04mol/L£¬
¹Ź“š°øĪŖ£ŗ0.4£»0.04£»
£Ø3£©¢ŁĻąĶ¬Ģõ¼žĻĀ£¬M”¢NĘųĢåµÄĆܶČÖ®±ČÓėĘäĦ¶ūÖŹĮæ³ÉÕż±Č£¬M”¢NĮ½ÖÖĘųĢ¬»ÆŗĻĪļ£¬ĘäĦ¶ūÖŹĮæÖ®±ČĪŖ4£ŗ3£¬ĖłŅŌ¶žÕßµÄĆܶČÖ®±ČĪŖ£ŗ4£ŗ3£¬
¹Ź“š°øĪŖ£ŗ4£ŗ3£»
¢ŚĮ½øöČŻĘ÷ÖŠĘųĢåµÄĆܶČĻąĶ¬£¬ŌņĘųĢåµÄÖŹĮæĻąµČ£¬ĪļÖŹµÄĮæÓėĦ¶ūÖŹĮæ³É·“±Č£¬¶ųŃ¹ĒæÓėĘųĢåµÄĪļÖŹµÄĮæ³ÉÕż±Č£¬ŌņČŻĘ÷ÖŠĘųĢåµÄŃ¹ĒæÓėĦ¶ūÖŹĮæ³É·“±Č£¬Į½øöČŻĘ÷ÖŠŃ¹ĒæÖ®±ČĪŖ£ŗ3£ŗ4£¬
¹Ź“š°øĪŖ£ŗ3£ŗ4£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪö”¢¼ĘĖćÄÜĮ¦µÄ漲飬עŅā°ŃĪÕĻą¹Ų¼ĘĖć¹«Ź½µÄŌĖÓĆŅŌ¼°ĪļÖŹµÄ¹¹³ÉĢŲµć£¬×¢ŅāÕĘĪÕĪļÖŹµÄĮæÓė°¢·üŁ¤µĀĀŽ³£Źż”¢Ä¦¶ūÖŹĮ攢ĪļÖŹµÄĮæÅØ¶ČµČĪļĄķĮæÖ®¼äµÄ×Ŗ»Æ¹ŲĻµ£¬ĢāÄæÄѶČÖŠµČ£®


 ŠÄĖćæŚĖćĒÉĖćŅ»æĪŅ»Į·ĻµĮŠ“š°ø
ŠÄĖćæŚĖćĒÉĖćŅ»æĪŅ»Į·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
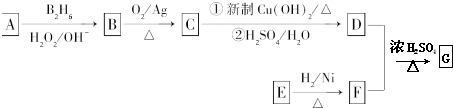
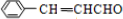 £®
£®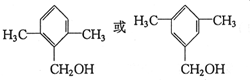 £®
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
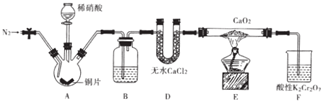
 ÄæĒ°°ėµ¼ĢåÉś²śÕ¹æŖĮĖŅ»³””°ĶŠ¾Ę¬”±øļĆü--ŌŚ¹čŠ¾Ę¬ÉĻÓĆĶ“śĢęĀĮ²¼Ļߣ¬¹ÅĄĻµÄ½šŹōĶŌŚĻÖ“śæĘ¼¼Ó¦ÓĆÉĻČ”µĆĮĖĶ»ĘĘ£®ÓĆ»ĘĶæó£ØÖ÷ŅŖ³É·ÖĪŖCuFeS2£©Éś²ś“ÖĶ£¬Ęä·“Ó¦ŌĄķČēĻĀ£ŗ
ÄæĒ°°ėµ¼ĢåÉś²śÕ¹æŖĮĖŅ»³””°ĶŠ¾Ę¬”±øļĆü--ŌŚ¹čŠ¾Ę¬ÉĻÓĆĶ“śĢęĀĮ²¼Ļߣ¬¹ÅĄĻµÄ½šŹōĶŌŚĻÖ“śæĘ¼¼Ó¦ÓĆÉĻČ”µĆĮĖĶ»ĘĘ£®ÓĆ»ĘĶæó£ØÖ÷ŅŖ³É·ÖĪŖCuFeS2£©Éś²ś“ÖĶ£¬Ęä·“Ó¦ŌĄķČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | °Ń½šŹōĢś·ÅČėĻ”ĮņĖįÖŠ£ŗ2Fe+6H+=2Fe3++3H2”ü | |
| B£® | ĶłĢ¼ĖįĆ¾ÖŠµĪ¼ÓĻ”ŃĪĖį£ŗMgCO3+2H+ØTCO2”ü+H2O+Mg2+ | |
| C£® | ĻņĒāŃõ»ÆĶÖŠµĪ¼ÓĻ”ŃĪĖį£ŗCu£ØOH£©2+2H+ØTCu2++2H2O | |
| D£® | ĒāŃõ»Æ±µČÜŅŗÓėĻ”ĮņĖį·“Ó¦£ŗBa2++SO42-+H++OH-ØTBaSO4”ż+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “óÓŚ10.0mL | B£® | Š”ÓŚ10.0mL | C£® | µČÓŚ10.0mL | D£® | µČÓŚ11.0mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HBr”¢HCl”¢HF | B£® | BaSO4”¢NH4Cl”¢CH3COONa | ||
| C£® | NaOH”¢Ca£ØOH£©2”¢NH3•H2O | D£® | HClO”¢CaCl2”¢SO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·²ŹĒŗ¬Ģ¼ŌŖĖŲµÄ»ÆŗĻĪļ¶¼ŹōÓŚÓŠ»ś»ÆŗĻĪļ | |
| B£® | Ņ×ČÜÓŚĘūÓĶ”¢¾Ę¾«”¢±½µČÓŠ»śČܼĮµÄĪļÖŹŅ»¶ØŹĒÓŠ»ś»ÆŗĻĪļ | |
| C£® | ĖłÓŠµÄÓŠ»ś»ÆŗĻĪļ¶¼Ņ×Č¼ÉÕ | |
| D£® | ÓŠ»ś»ÆŗĻĪļµÄĶ¬·ÖŅģ¹¹ĻÖĻóŹĒÓŠ»ś»ÆŗĻĪļÖÖĄą·±¶ąµÄÖŲŅŖŌŅņÖ®Ņ» |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øƵē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗó£¬KOHČÜŅŗµÄÖŹĮæ·ÖŹż²»±ä | |
| B£® | ¹©µēŹ±µÄ×Ü·“Ó¦ĪŖ£ŗ2H2+O2$\frac{\underline{\;µćČ¼\;}}{\;}$2H2O | |
| C£® | ĒāŃõČ¼ĮĻµē³ŲÖŠH2ŗĶO2Č¼ÉշųöµÄČČĮæ×Ŗ±äĪŖµēÄÜ | |
| D£® | øĆČ¼ĮĻµē³ŲæÉŅŌÓĆĮ½øö»īŠŌĻąĶ¬µÄµē¼« |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com