

 ;NO2+与CO2互为等电子体,二者结构相似,故NO2+的电子式为
;NO2+与CO2互为等电子体,二者结构相似,故NO2+的电子式为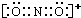 ;基态Cu原子的核外电子排布简式为[Ar]3d104s1,
;基态Cu原子的核外电子排布简式为[Ar]3d104s1, ;
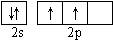
;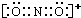 ;[Ar]3d104s1;
;[Ar]3d104s1;| 1 |
| 4 |
| 4 |
| 3 |
| 4 |
| 3 |
| 16 |
| 3 |
| ||
| 8(a+b)3 |
| 2π(a3+b3) |
| 3(a+b)3 |
| 2π(a3+b3) |
| 3(a+b)3 |


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
| A、SO2通入溴水中:SO2+2H2O+Br2═2H++SO42-+2HBr |
| B、向硫酸氢铵溶液中加入少量氢氧化钠溶液:NH4++OH-═NH3?H2O |
| C、硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| D、过量稀硝酸和铁屑反应:Fe+4H++NO3-═Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、保存浓硝酸时,通常用棕色瓶并放在阴凉处 |
| B、用纯锌与稀硫酸反应制取氢气时,在溶液中加入少量硫酸铜溶液 |
| C、合成氨的反应中,选择“铁触媒”作催化剂 |
| D、在试管中进行铝和氢氧化钠溶液反应时,稍微加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 难溶物[ | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| CaSO4 | 9.1×10-6 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 废水浓度 | 29.4g/L | 1.6g?L-1 |
| 排放标准 | pH 6~9 | 0.5mg?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 压强/Mpa/体积分数/%/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 82.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl=H2SO4>CH3COOH |
| B、HCl>H2SO4>CH3COOH |
| C、H2SO4>HCl>CH3COOH |
| D、HCl=H2SO4=CH3COOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com