
| A. | 合金不能导电、传热 | B. | 合金没有延展性 | ||
| C. | 合金属于化合物 | D. | 合金的许多性能与其组成成分不同 |
分析 合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质.合金概念有三个特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属.铝合金具有优良的导电性、导热性和抗蚀性,因此合金也导电.
解答 解:A.铝合金具有优良的导电性、导热性和抗蚀性,因此合金也导电;故A错误;
B.合金也有延展性,故B错误;
C.合金属于混合物,不是化合物,故C错误;
D.合金的许多性能与组成它们的成分不同,如合金的硬度大,熔点低,耐腐蚀,故D正确;
故选D.
点评 本题主要考查合金与合金的性质,合金概念的三个特点要记牢;还要理解合金的性质,即合金的硬度大,熔点低,耐腐蚀,题目难度不大.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:解答题
| 实验序号 |  | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
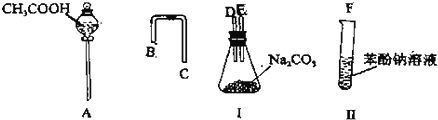
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ”结构存在的同分异构体的数目有( )
”结构存在的同分异构体的数目有( )| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中X位于Y的上一周期 | |
| B. | X的含氧酸的酸性强于Y的含氧酸的酸性 | |
| C. | 将H2X、HY分别加热至500℃,只有HY发生分解 | |
| D. | Xn-的还原性强于Ym- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| D. | 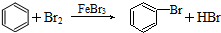 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
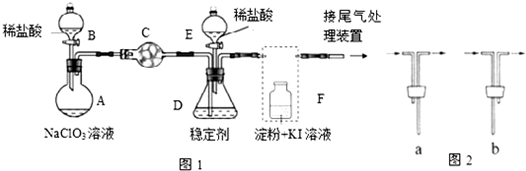
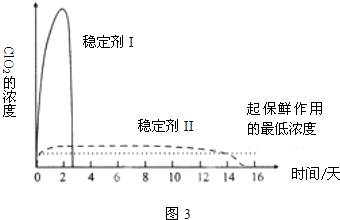
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com