
| A. | 若E、F、W形成的化合物EFW2,则E与W可以形成化合物E2W2 | |
| B. | F的最高价氧化物对应的水化物一定能与氢氧化钠溶液反应 | |
| C. | 稳定性:Z的氢化物>W的氢化物 | |
| D. | 沸点:Z的氢化物>W的氢化物 |
分析 E、F、Z、W为短周期元素,E是短周期中除稀有气体元素外半径最大的元素,则E为Na;E、F、Z处于同一周期,E、F、Z原子序数之和为40,则F、Z的原子序数之和=40-11=29,原子半径E>F>Z>W,F可能为Mg、Al、Si,对应的Z可能为Cl、S、P,由于Z、W处于同一主族,相应的W为F、O、N,据此解答.
解答 解:E、F、Z、W为短周期元素,E是短周期中除稀有气体元素外半径最大的元素,则E为Na;E、F、Z处于同一周期,E、F、Z原子序数之和为40,则F、Z的原子序数之和=40-11=29,原子半径E>F>Z>W,F可能为Mg、Al、Si,对应的Z可能为Cl、S、P,由于Z、W处于同一主族,相应的W为F、O、N,
A、若E、F、W形成的化合物EFW2,则为NaAlO2,则钠与氧可以形成化合物Na2O2,故A正确;
B、如果F是镁,最高价氧化物对应的水化物氢氧化镁不与氢氧化钠反应,故B错误;
C、Z的非金属弱于W的非金属性,所以Z的氢化物<W的氢化物,故C错误;
D、如果Z是硫,则W是氧,它们氢化物分别是硫化氢和水,水分子间存在氢键,所以沸点:Z的氢化物<W的氢化物,故D错误;
故选A.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意元素的不确定性,难度中等.


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度时,在2L容器中A、B、C三种物质的物质的量浓度随时间变化关系曲线如图所示.
某温度时,在2L容器中A、B、C三种物质的物质的量浓度随时间变化关系曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )
2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )| A. | 该反应的反应物总能量小于生成物总能量 | |
| B. | 该反应的逆反应为吸热反应 | |
| C. | 图中△H=-99kJ•mol-1, | |
| D. | 图中字母E所示能量值表示该反应的活化能 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
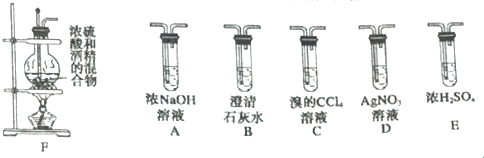
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/K | 473 | 573 | 673 | … |
| K | 4.4×10-2 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水晶有固定的熔点,而普通玻璃则没有 | |
| B. | 水泥、玻璃、陶瓷属于传统的无机非金属材料 | |
| C. | 不锈钢和普通钢的组成元素完全相同,但耐腐蚀性能不同 | |
| D. | 氯化铵和单质碘在加热时有类似现象,但本质不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | N2O4(g)?2NO2(g) | B. | CO2(g)+C(s)?2CO(g) | ||
| C. | 2SO2(g)+O2(g)?2SO3(g) | D. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com