
下列既属于氧化还原反应,又属于吸热反应的是
A.铝片和稀盐酸反应
B.高温煅烧石灰石
C.灼热的碳与二氧化碳的反应
D.甲烷在氧气中的燃烧
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
A、B、C是三种短周期元素,其中A元素原子M层上电子数比L层少2个电子;B元素原子比A元素原子的电子层少,又知B元素最高正价与负化合价的绝对值相等;C 元素的阳离子核外电子排布与Ne原子核外电子排布相同;且又知这三种元素可组成BA2型共价化合物和C2A型离子化合物。由上述条件回答下列问题:
(1)A、B、C三元素的名称分别是:A_______,B_______,C_______。
(2)化合物C2A的电子式是______________,
(3)化合物BA2的电子式是:______________,结构式是:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
把质量为mg的铜丝灼烧变黑,立即放入下列物质中,使铜丝变红,而且质量仍为mg
的是 ( )
①稀硫酸 ②C2H5OH ③稀硝酸 ④CO
A.①② B.②④ C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列各溶液中,离子一定能大量共存的是( )
A.强酸性溶液中:K+、Al3+、CH3COO-、SO42-
B.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO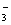 、Br-、Ba2+
、Br-、Ba2+
C.室温下,pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl-
D.室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下: TaS2(g)+ 2I2(g)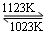 TaI4(g) + S2(g),下列说法错误的是( )
TaI4(g) + S2(g),下列说法错误的是( )
A.在不同温度区域,TaI4 的量不同
B.在提纯过程中,S2 的量不断增多
C.该反应的平衡常数不随TaI4 和S2 的浓度增大而增大
D.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示方法正确的是
A. 氨气的燃烧热为-316.3kJ·mol-1,则氨气燃烧的热化学方程式可表示为:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H= -316.3kJ·mol-1
B. 500℃、30MPa下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中充分反应
NH3(g),放热19.3kJ,其热化学方程式为:
N2 (g) + 3H2(g)  2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C. 由C(石墨)= C(金刚石)△H=+1.90kJ·mol-1 ,可知金刚石比石墨稳定
D. 由H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,可知将含0.5molH2SO4的浓溶液
与含1molNaOH的稀溶液混合,放出的热量大于57.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1×105 Pa,298 K条件下2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1
蒸发1g H2O (l)需要吸收的能量为2.5 kJ,其他数据如下表:
| H2(g) | O2(g) | H2O(l) | |
| 1 mol分子中的化学键 断裂时需要吸收的能量/kJ | 436 | 746 | a |
则表中a为
A.350 B.548 C.1096 D.2192
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,向一体积为2L的恒容密闭容器中充入2mol A,1mol B,发生如下反应:
2A(g)+B  3C(g);△H=-QkJ/mol(Q>0)。经过60s达到平衡,测得B物质的量
3C(g);△H=-QkJ/mol(Q>0)。经过60s达到平衡,测得B物质的量
为0.2mol,下列对该平衡的叙述正确的是 ( )
A.用C的浓度变化表示该反应速率为2.4mol.L-1.min-1
B.若使容器变为1L,则C的物质的量一定增大
C.达到平衡,测得放出热量为xkJ,则x=Q
D.若向容器再充入1mol C,重新达到平衡,A的体积分数保持不变,则B为气态
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.Al、Fe、Cu三者对应的氧化物均为碱性氧化物
B.向污水中投放明矾,能生成凝聚悬浮物的Al(OH)3胶体,起到净水的作用
C.向NaAlO2溶液中通入过量CO2:2AlO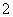 +CO2+3H2O===2Al(OH)3↓+CO
+CO2+3H2O===2Al(OH)3↓+CO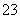
D.加入铝粉能产生H2的溶液中,一定存在大量的Na+、Ba2+、AlO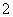 、Cl
、Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com