
某烷烃的结构简式为
(1)用系统命名法命名该烃:_______________________________________________________。
(2)若该烷烃是由烯烃和1 mol H2加成得到的,则原烯烃的结构有__________种。(不包括立体异构,下同)
(3)若该烷烃是由炔烃和2 mol H2加成得到的,则原炔烃的结构有__________种。
(4)该烷烃在光照条件下与氯气反应,生成的一氯代烷最多有__________种。
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25 ℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如下:
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为____________________。
(2)向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10-10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=__________。
②完全沉淀后,溶液的pH=__________。
③如果向完全沉淀后的溶液中继续加入50 mL 0.001 mol·L-1的盐酸,是否有白色沉淀生成?________________(填“是”或“否”)。
(3)在某温度下,Ksp(FeS)=6.25×10-18,FeS饱和溶液中c(H+)与c(S2-)之间存在关系:c2(H+)·c(S2-)=1.0×10-22,为了使溶液里c(Fe2+) 达到1 mol·L-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等。它们的最高价氧化物的水化物依次为甲、乙、丙、丁。下列叙述不正确的是:

A.R的氧化物在空气中与其它物质作用可形成光化学烟雾
B.常温下丁的浓溶液可用T单质所制的容器来盛装
C.丁的浓溶液与Q的单质加热发生反应,可生成体积比为1:2的两种气体
D.甲、乙、丙、丁受热均易分解
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-具有相同的电子层结构,下列叙述不正确的是 ( )
A.离子半径A2->C->B2+ B.它们的原子序数A>B>C
C.它们的原子半径C>B>A D.原子最外层上的电子数B>A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W四种短周期元素,原子序数依次增大。且Y、Z、W为同周期元素,X、Z同主族,X、Z可形成共价化合物ZX3 和ZX2 ,
Y的原子结构示意图右图,据此填空:
(1)Y的元素名称为 。
(2)X、Y、Z三种元素的原子,半径由小到大的顺序为 (用元素符号表示)。
(3)Y和W最高价氧化物的水化物酸性由强到弱的顺序为 (用化学式表示)。
(4)已知Na和单质Z可以形成离子化合物,写出该物质的电子式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填写下列空白
(1)CH3CHCH2+( )—→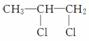 ,反应类型:________。
,反应类型:________。
 (2)CH3CHCH2+Cl2500℃~600℃,( )+HCl,反应类型:________。
(2)CH3CHCH2+Cl2500℃~600℃,( )+HCl,反应类型:________。
(3)CH2CHCHCH2+( )—→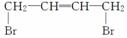 ,反应类型:________。
,反应类型:________。
(4)( )+Br2—→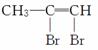 ,反应类型:____________。
,反应类型:____________。
(5)( )一定条件, 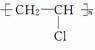 ,反应类型:____________。
,反应类型:____________。
(6)CH3CHCH2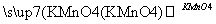 CH3COOH+
CH3COOH+
( ),反应类型:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
近日国内知名山茶油品牌“金浩茶油”被多家媒体曝光致癌物苯并(a)芘含量超标。苯并(a)芘是一种致癌物、致畸原及诱变
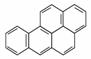
剂,也是多环芳烃中毒性最大的一种强致癌物。苯并(a)芘的结构简式如图所示,下列有关苯并(a)芘的说法中不正确的是( )
A.苯并(a)芘的分子式为C20H12,属于稠环芳香烃
B.苯并(a)芘与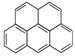 互为同分异构体
互为同分异构体
C.苯并(a)芘在一定条件下可以发生取代反应,但不能使酸性KMnO4溶液褪色
D.苯并(a)芘不易溶于水,易溶于苯、氯仿等有机溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4,其流程如下:

已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:13℃)。
(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是_____,原 料中的金属钠通常保存在____中,实验室取用少量金属钠需要用到的实验用品有_____,_____,玻璃片和小刀等。
料中的金属钠通常保存在____中,实验室取用少量金属钠需要用到的实验用品有_____,_____,玻璃片和小刀等。
(2)请配平第①步反应的化学方程式:
□NaBO2+□SiO2+□Na+□H2----- --□NaBH4+□Na2SiO3
--□NaBH4+□Na2SiO3
(3)第②步分离采用的方法是______;第③步分离(NaBH4)并回收溶剂,采用的方法是______。
(4)NaBH4(s)与水(l)反应生成NaBO2(s)和氢气(g),在25℃,101KPa下,已知每消耗3.8克NaBH4(s)放热21.6KJ,该反应的热化学方程式是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com