
【题目】下列有关说法正确的是
A.电解质溶液导电为化学变化
B.Na、SiO2、H2O都称为分子式
C.NH3的水溶液能导电,所以NH3为电解质
D.HClO、KNO3、H2O2中均含离子键
科目:高中化学 来源: 题型:
【题目】如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).已知:pAg=﹣lg{c(Ag+)},Ksp(AgCl)=1×10﹣12 . 根据图象所得下列结论正确的是( )(提示:Ksp(AgCl)>Ksp(AgI)) 
A.原AgNO3溶液的物质的量浓度为0.1 molL﹣1
B.图中x点的坐标为(100,6 )
C.图中x点可认为溶液中Ag+被沉淀完全
D.把0.1 molL﹣1的NaCl换成0.1 molL﹣1NaI则图象在终点后变为虚线部分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组欲通过实验方法验证Fe2+的某些性质.
(1)在实验前,依据Fe2+的性,填写了如表.
实验操作 | 预期现象 | 反应的离子方程式 |
向盛有新割FeSO4溶液的试管中滴入数滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液颜色逐渐变黄 | Fe2++NO3﹣+2H+=Fe3++NO2↑+H2O |
依照表中操作,该小组进行实验.观察到液面上方气体逐渐变为红棕色,但试管中溶液颜色却变为深棕色.
(2)分别取少量反应后的溶液于两只试管中,一只滴加几滴KSCN溶液,溶液变为变红,则溶液中含有;另一只试管滴加几滴溶液,产生蓝色沉淀,则含有Fe2+ .
(3)该小组讨论认为深棕色可能是NO2或NO与铁的某一种离子发生反应引起的.
提出猜想:
ⅰ.NO2与Fe2+发生反应ⅱ.NO2 与Fe3+发生反应
ⅲ.NO与Fe2+发生反应ⅳ.
(4)该小组用如图装置进行探究: 
步骤 | 操作及现象 | 解释或结论 |
① | 关闭k、b,打开a,开始甲中反应,一段时间后,观察到丙中溶液逐渐变为深棕色,而丁中溶液无明显变化 | 溶液深棕色由与NO或NO2反应而的得到 |
② | 停止甲中反应,打开k、b,关闭a,持续通入N2一段时间 | 该操作的目的 |
③ | 更换新的丙、丁装置,再通一段时间N2后关闭k,使甲中反应继续,观察到的现象与步骤①中相同 | 乙瓶中发生的化学反应方程式为 |
(5)结合实验猜想,得出结论:
溶液呈深棕色的原因:肯定成立的是猜想;不确定的是猜想 , 有待后续实验进一步探究.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氮的固定作用的是
A. N2和H2一定条件下反应制取NH3 B. 硝酸工厂用NH3氧化制取NO
C. NO遇空气转化为NO2 D. 由NH3制碳酸氢铵和硫酸氨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
A.②、⑧、⑨对应的简单离子半径依次增大
B.⑥的氯化物的熔点比⑦的氯化物熔点高
C.元素⑩处于常见周期表第四周期第VIIIB族
D.①分别与③、④、⑤均可形成既含极性键又含非极性键的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)2017年1月2日安徽六安出现了严重雾霾情况,经分析该雾霾中含有大量PM2.5、PM10、汽车尾气等等.将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42﹣ | NO3﹣ | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣6 | 2×10﹣5 | 4×10﹣5 | 3×10﹣5 | 2×10﹣5 |
根据表中数据判断PM2.5试样的pH= .
(2)在一定条件下的溶液中,反应FeCl3+3KSCNFe(SCN)3+3KCl达到平衡后,在其他条件不变的情况下,加入少量KCl固体,能使平衡移动(填“正向”、“逆向”、“不”)
(3)泡沫灭火器是硫酸铝和碳酸氢钠溶液反应,反应的离子方程式是 .
(4)常温下,一定体积PH=2的二元弱酸H2R溶液与等体积PH=12的NaOH溶液混合,该混合溶液中电荷守恒的关系式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍具有优良的物理和化学特性,是高技术产业的重要原料. 羰基法提纯镍涉及的反应为:Ni(s)+4CO(g)Ni(CO)4(g)
①当温度升高时, ![]() 减小,则△H0(填“>”或“<”).
减小,则△H0(填“>”或“<”).
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是(填代号)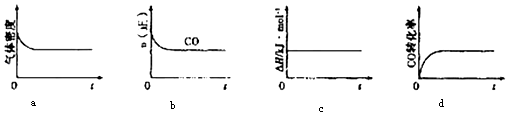
在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数(填“增大”、“不变”或“减小”),反应进行3s后测得Ni(CO)4的物质的量为0.6mol,则0﹣3s内的平均反应速率v(CO)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验和分析正确的是( )
A.无色溶液中加入AgNO3溶液得白色沉淀,加稀盐酸不消失,可能存在Cl﹣或SO ![]()
B.无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸不溶解,则一定含有SO ![]()
C.用CCl4萃取碘水中的碘,下层呈紫红色
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有大量CO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含CuSO4和H2SO4的混合溶液200mL,其中CuSO4物质的量浓度为1molL﹣1 , H2SO4物质的量浓度为0.5molL﹣1 , 若用此溶液配成0.2molL﹣1 CuSO4和2molL﹣1 H2SO4的混合溶液,试求:
(1)所得溶液的体积是多少毫升?
(2)需加入密度为1.84gcm﹣3、98%的浓硫酸多少毫升?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com