

���� ��1����2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ•mol-1
��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ•mol-1�����ø�˹���ɽ��١�$\frac{1}{2}$-�ڡ�$\frac{1}{2}$����õ���
��2�����ݴﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ɴ�������һЩ������Ҳ���䣻����ƽ��ʱ�����ʵ�Ũ�ȣ��ɼ���ƽ�ⳣ����
��3�����û�ѧƽ���Ӱ�����غ�ҵ�����Ĺ�ϵ��������
��� �⣺��1����֪����2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ•mol-1
��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ•mol-1�����ø�˹���ɽ��١�$\frac{1}{2}$-�ڡ�$\frac{1}{2}$��NO2��g��+SO2��g��?SO3��g��+NO��g��
��H=$\frac{1}{2}$����-196.6kJ•mol-1��-$\frac{1}{2}$����-113.0kJ•mol-1��=-41.8kJ•mol-1���ʴ�Ϊ��-41.8��
��2��a�������Ƿ�ﵽƽ�⣬��ϵѹǿ�����ֲ��䣬���������ж��Ƿ�ﵽƽ��״̬����a����
b�����������ɫ���ֲ��䣬˵��Ũ�Ȳ��䣬�ﵽƽ��״̬����b��ȷ��
c��SO3��NO�ļ�����֮��Ϊ1��1�������Ƿ�ﵽƽ�⣬���ߵ�����ȱ��ֲ��䣬�����ж��Ƿ�ﵽƽ��״̬����c����
d�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ���ÿ����1mol SO3��ͬʱ����1molNO2�������ж��Ƿ�ﵽƽ��״̬����d����
NO2��g��+SO2��g��?SO3��g��+NO��g��
��ʼ���ʵ���� a 2a 0 0
ת�����ʵ���� x x x x
ƽ�����ʵ���� a-x 2a-x x x
ƽ��ʱNO2��SO2�����Ϊ1��6������1a-x������2a-x��=1��6����x=$\frac{4}{5}$a����ƽ�ⳣ��K=$\frac{c��SO{\;}_{3}��c��NO��}{c��NO{\;}_{2}��c��SO{\;}_{2}��}$=$\frac{x{\;}^{2}}{��a-x����2a-x��}$=$\frac{\frac{16}{25}a{\;}^{2}}{\frac{1}{5}a��\frac{6}{5}a}$=$\frac{8}{3}$��
�ʴ�Ϊ��b��$\frac{8}{3}$��
��3����ͼ��֪���¶����ߣ�CO��ת���ʽ��ͣ�ƽ�����淴Ӧ�����ƶ������淴Ӧ�����ȷ�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����H��0��ѹǿ�������ڼӿ췴Ӧ���ʣ�������ʹƽ�������ƶ�����ѹǿ������Ҫ�Ķ������豸��Ҫ��Ҳ�ߣ���ѡ��250�桢1.3��104kPa���ҵ���������Ϊ��250�桢ѹǿΪ1.3��104 kPaʱ��CO��ת�����ѽϴ�������ѹǿ��CO��ת���ʱ仯����û�б�Ҫ������ѹǿ��
�ʴ�Ϊ��������1.3��104kPa�£�CO��ת�����ѽϸߣ�������ѹǿCO��ת������߲��������ɱ����ӵò���ʧ��
���� ������NO2��SO2��CO������Ϊ���壬�ۺϿ��黯ѧƽ���ƶ�����˹�����Լ�������⣬������ѧ���ۺ����û�ѧ֪ʶ�������Ŀ��飬��Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mo1 Na2O2������H2O��Ӧ��ת����2 NA ������ | |
| B�� | 1 mol O2�ڷ�Ӧ�еõ�������һ��Ϊ4 NA | |
| C�� | 1 mol Cl2�ڷ�Ӧ�еõ���������һ��Ϊ2NA | |
| D�� | ��2KClO3+4HC1��Ũ���T2KCl+2C1O2��+C12��+2H2O�У��������������������ǻ�ԭ���ÿ����1 mol Cl2ת��2 NA ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2��3��2 | B�� | 2��2��3 | C�� | 1��3��4 | D�� | 3��1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl- | B�� | F - | C�� | S2- | D�� | Br |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
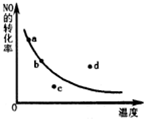 ��֪��Ӧ��2NO+O2?2NO2��H��0����ͼ�����DZ�ʾ��������һ��ʱ����Ӧ��NO���ת�������¶ȵĹ�ϵ���ߣ�ͼ�б���a��b��c��d�ĵ㣬���б�ʾδ�ﵽƽ��״̬����v��������v���棩�ĵ��ǣ�������
��֪��Ӧ��2NO+O2?2NO2��H��0����ͼ�����DZ�ʾ��������һ��ʱ����Ӧ��NO���ת�������¶ȵĹ�ϵ���ߣ�ͼ�б���a��b��c��d�ĵ㣬���б�ʾδ�ﵽƽ��״̬����v��������v���棩�ĵ��ǣ�������| A�� | a�� | B�� | b�� | C�� | c�� | D�� | d�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ҵ������Ȼ�̼ | B�� | �����屽�����Ȼ�̼ | ||
| C�� | ���������Ҵ������Ȼ�̼ | D�� | ���������Ҵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ϊ��ȥ���еı��ӣ��ɼ���������ˮ��Һ���ٹ��� | |
| B�� | Ϊ��ȥFeSO4��Һ�е�Fe2��SO4��3���ɼ������ۣ��ٹ��� | |
| C�� | Ϊ��ȥ��Ȳ����������H2S����ʹ��ͨ��CuSO4��Һ | |
| D�� | Ϊ��ȥCO2��������SO2����ʹ��ͨ������NaHCO3��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com