
| A. | 150mL 1mol•L-1的NaCl溶液 | B. | 75 mL 3 mol•L-1 NH4Cl溶液 | ||
| C. | 150 mL 2 mol•L-1的KCl溶液 | D. | 75 mL 2mol•L-1的FeCl3溶液 |
分析 50mL1mol/L的AlCl3溶液中的Cl-浓度为3mol/L,根据溶质化学式计算各选项中的Cl-物质的量,进行比较可知.注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.
解答 解:50mL 1mol•L-1 AlCl3溶液中Cl-物质的量浓度是1mol/L×3=3mol/L,
A.150mL 1mol•L-1氯化钠溶液中c(Cl-)=1 mol•L-1×1=1mol/L,故A错误;
B.75ml 3mol•L-1NH4Cl溶液中Cl-浓度3mol/L,故B正确;
C.150 mL 2 mol•L-1的KCl溶液中c(Cl-)=2mol•L-1×1=2mol/L,故C错误;
D75 mL 2mol•L-1的FeCl3溶液中c(Cl-)=2mol•L-1×3=6mol/L,故D错误.
故选B.
点评 本题考查物质的量浓度的相关计算,为高频考点,注意“溶液中离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数进行计算,与溶液的体积无关”,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 医疗中用75%的乙醇溶液进行消毒,是由于蛋白质遇酒精会变性 | |
| B. | 臭氧可用于自来水消毒,是因为臭氧具有强氧化性能杀死水中的病菌 | |
| C. | 腌制熟食品时,添加少量NaNO2,是为了使其味道更加美味可口 | |
| D. | 食盐中加入少量碘酸钾,食用后可补充人体内碘元素的不足 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
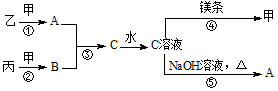 甲、乙、丙均为中学化学常见的气体单质,A为10电子化合物,B为18电子化合物,各物质之间存在如图所示的转化关系(部分反应条件及产物略去):
甲、乙、丙均为中学化学常见的气体单质,A为10电子化合物,B为18电子化合物,各物质之间存在如图所示的转化关系(部分反应条件及产物略去): .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯与HBr反应 | B. | 1,3-丁二烯与溴以1:1反应 | ||
| C. | 苯与液溴混合物中加入铁粉 | D. | 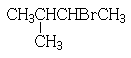 与KOH的醇溶液反应 与KOH的醇溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在元素周期表金属与非金属的分界处可以寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| B. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| C. | 水分子很稳定,是因为水中存在氢键 | |
| D. | 在多电子的原子里,能量高的电子通常在离核远的区域内活动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度不再变化 | B. | 反应容器中Y的质量分数不变 | ||
| C. | 体系压强不再变化 | D. | Z的浓度不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl- | B. | Na+ | C. | H+ | D. | Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com